reglas para determinar prioridades
estas reglas se conocen como reglas Cahn-Ingold-Prelog (CIP) por las personas que desarrollaron el sistema.
la primera regla para casos muy simples
primero observas los átomos unidos directamente a los átomos de carbono en cada extremo del doble enlace, pensando en los dos extremos por separado.
-
el átomo que tiene el número atómico más alto se le da la prioridad MÁS ALTA.
veamos el ejemplo que hemos estado hablando.,

simplemente considere el primer isómero y mire por separado el átomo de carbono izquierdo y luego el derecho. Compare los números atómicos de los átomos unidos para resolver las diversas prioridades.
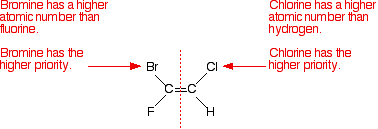
Observe que los átomos con las más altas prioridades están ambos en el mismo lado del doble enlace. Eso cuenta como el isómero (Z).
el segundo isómero obviamente todavía tiene los mismos átomos en cada extremo, pero esta vez los átomos de mayor prioridad están en lados opuestos del doble enlace. Ese es el isómero (E).,
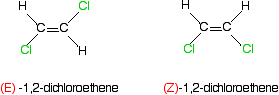
¿Qué pasa con los ejemplos más familiares como 1,2-dicloroeteno o but-2-ENO? Aquí está el 1,2-dicloroeteno.

piense en la prioridad de los dos grupos en el primer carbono del isómero izquierdo.
El cloro tiene un número atómico más alto que el hidrógeno, y por lo tanto tiene la prioridad MÁS ALTA. Eso, por supuesto, es igualmente cierto para todos los otros átomos de carbono en estos dos isómeros.
en el primer isómero, los grupos de mayor prioridad están en lados opuestos del enlace. Ese debe ser el isómero (E)., El otro, con los grupos de mayor prioridad en el mismo lado, es el isómero (Z).
Y ahora but-2-eno . . .
esto añade la ligera complicación de que no tienes un solo átomo unido al doble enlace, sino un grupo de átomos.
Eso no es un problema. Concéntrese en el átomo directamente unido al doble enlace , en este caso el carbono en el grupo CH3. Para este caso simple, puede ignorar completamente los átomos de hidrógeno en el grupo CH3., Sin embargo, con grupos más complicados es posible que tenga que preocuparse por los átomos que no están directamente Unidos al doble enlace. Veremos ese problema en un momento.
Aquí está uno de los isómeros de but-2-ENO:

el grupo CH3 tiene la prioridad MÁS ALTA porque su átomo de carbono tiene un número atómico de 6 en comparación con un número atómico de 1 para el hidrógeno también unido al doble enlace carbono-carbono.
el isómero dibujado arriba tiene los dos grupos de mayor prioridad en lados opuestos del doble enlace. El compuesto es (E) – but-2-ENO.,
una adición menor a la regla para permitir isótopos de, por ejemplo, hidrógeno
deuterio es un isótopo de hidrógeno que tiene una masa atómica relativa de 2. Todavía tiene solo 1 protón, y por lo tanto todavía tiene un número atómico de 1. Sin embargo, no es lo mismo que un átomo de hidrógeno «ordinario», por lo que estos dos compuestos son isómeros geométricos:

El hidrógeno y el deuterio tienen el mismo número atómico, por lo que sobre esa base, tendrían la misma prioridad., En un caso como ese, el que tiene la masa atómica relativa más alta tiene la prioridad MÁS ALTA. Así que en estos isómeros, el deuterio y el cloro son los grupos de mayor prioridad en cada extremo del doble enlace.
eso significa que el isómero izquierdo en el último diagrama es la forma (E), y el de la derecha la (Z) -.
extender las reglas a moléculas más complicadas
si estás leyendo esto porque estás haciendo un curso para niños de 16 a 18 años como UK a level, es posible que no necesites saber mucho sobre esta sección, ¡pero realmente no es muy difícil!,
ilustremos esto tomando una molécula de aspecto bastante aterrador, y viendo lo fácil que es averiguar si es un isómero (Z) o (E) aplicando una regla adicional.
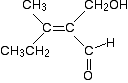
en el extremo izquierdo de la molécula. ¿Qué está unido directamente al doble enlace carbono-carbono?
en ambos grupos unidos, un átomo de carbono está unido directamente al enlace. Esos dos átomos obviamente tienen el mismo número atómico y por lo tanto la misma prioridad. Así que eso no ayuda.,
en este tipo de casos, ahora miras lo que está unido directamente a esos dos carbonos (pero sin contar el carbono del doble enlace) y comparas las prioridades de estos siguientes átomos.
Puede hacer esto en su cabeza en casos simples, pero a veces es útil escribir los átomos adjuntos, enumerándolos con el átomo de mayor prioridad primero. Los hace más fáciles de comparar. Así . . .
En el grupo CH3:
Los átomos unidos al carbono son H H H.
En el CH3CH2 grupo:
Los átomos conectados directamente con el carbono del grupo CH2 C H H.,
en la segunda lista, la C se escribe primero porque tiene el número atómico más alto.
Ahora compare las dos listas átomo por átomo. El primer átomo en cada lista es un H en el grupo CH3 y un C En el grupo CH3CH2. El carbono tiene la prioridad MÁS ALTA porque tiene el número atómico más alto. Por lo que da el grupo CH3CH2 una prioridad MÁS ALTA que el grupo CH3.
Ahora mira el otro extremo del doble enlace. Lo extra que esto ilustra es que si tienes un enlace doble, cuentas el átomo adjunto dos veces. Aquí está la estructura de nuevo.,

así que, de nuevo, los átomos unidos directamente al doble enlace carbono-carbono son ambos carbonos. Por lo tanto, tenemos que mirar lo que está unido a esos carbonos.
en el grupo CH2OH:
los átomos unidos directamente al carbono son O H H.
en el grupo CHO:
los átomos unidos directamente al carbono son O O H. recuerde que el oxígeno se cuenta dos veces debido al doble enlace carbono-oxígeno.
en ambas listas, los oxígenos se escriben primero porque tienen un número atómico más alto que el hidrógeno.,
entonces, ¿cuál es la prioridad de los dos grupos? El primer átomo en ambas listas es un oxígeno-eso no ayuda. Mira el siguiente átomo en ambas listas. En el grupo CH2OH, es un hidrógeno; en la lista CHO, es un oxígeno.
el oxígeno tiene la prioridad más alta-y eso le da al grupo CHO una prioridad MÁS ALTA que el grupo CH2OH.
el isómero es por lo tanto una (Z)- forma, porque los dos grupos de mayor prioridad (el grupo CH3CH2 y el grupo CHO) están ambos en el mismo lado del enlace.
esa ha sido una explicación bastante larga solo para dejar claro cómo funciona., Con un poco de práctica, se tarda unos segundos en trabajar en cualquier caso, excepto en los más complejos.
Un ejemplo más para hacer un par de puntos menores adicionales . . .
Aquí hay una molécula aún más complicada!
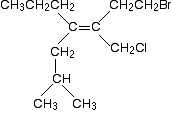
Antes de que siga leyendo, tener un ir en la elaboración de las prioridades relativas de los dos grupos en el extremo izquierdo de la doble enlace, y los dos en el extremo derecho., Hay otro poco de regla que no te he dicho específicamente todavía, pero no es difícil adivinar lo que podría ser cuando empiezas a mirar el problema. Si puedes resolver esto, entonces no tendrás ninguna dificultad con ningún problema que probablemente te encuentres en este nivel.
mira primero los grupos de la izquierda.
tanto en los grupos superior e inferior, tienes un grupo CH2 unido directamente al doble enlace carbono-carbono, y el carbono en ese grupo CH2 también está unido a otro átomo de carbono. En cada caso, la lista será C H H.,
no hay diferencia entre las prioridades de esos grupos, así que ¿qué vas a hacer al respecto? La respuesta es moverse a lo largo de la cadena al siguiente grupo. Y si es necesario, continúe haciendo esto hasta que haya encontrado una diferencia.
siguiente a lo largo de la cadena en la parte superior izquierda de la molécula es otro grupo CH2 unido a otro átomo de carbono. La lista para este grupo es de nuevo C H H.
pero el siguiente grupo a lo largo de la cadena en la parte inferior izquierda es un grupo CH unido a dos átomos de carbono más. Por lo tanto, su lista es C C H.,
comparar estas listas átomo por átomo, te lleva al hecho de que el grupo inferior tiene la prioridad MÁS ALTA.
Ahora mira los grupos de la derecha. Aquí está la molécula de nuevo:

El grupo superior derecho tiene C H H unido al primer carbono de la cadena.
El inferior derecho tiene Cl H H.
el cloro tiene un número atómico más alto que el carbono, por lo que el grupo inferior derecho tiene la prioridad MÁS ALTA de estos dos grupos.,
el punto extra que estoy tratando de hacer con este poco del ejemplo es que solo debe centrarse en un poco de una cadena a la vez. Nunca llegamos a considerar el bromo en el extremo superior derecho de la molécula. No necesitamos ir tan lejos a lo largo de la cadena – usted trabaja un eslabón a la vez hasta que encuentre una diferencia. Cualquier cosa más allá de eso es irrelevante.
para el registro, esta molécula es un isómero a (Z) porque los grupos de mayor prioridad en cada extremo están en el mismo lado del doble enlace.,
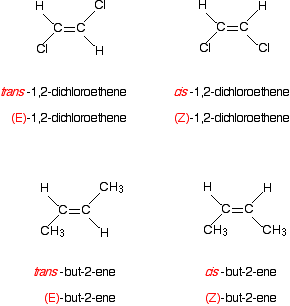
¿puede traducir fácilmente cis – y trans – en (Z)- y (E)-?
podría pensar que para casos simples, cis – solo se convertirá en (Z) – y trans-en (E) -.
Observe, Por ejemplo, los casos de 1,2-dicloroeteno y but-2-ENO.
Pero no siempre funciona! Piense en esta molécula relativamente sencilla . . .
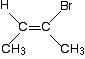
Este es claramente un cis isómero. Tiene dos grupos CH3 en el mismo lado del doble enlace. Pero resuelve las prioridades en el extremo derecho del doble enlace.,
los dos átomos directamente Unidos son carbono y bromo. El bromo tiene el número atómico más alto y por lo tanto tiene la prioridad MÁS ALTA en ese extremo. En el otro extremo, el grupo CH3 tiene la prioridad MÁS ALTA.
eso significa que los dos grupos de mayor prioridad están en lados opuestos del doble enlace, y por lo tanto este es un isómero (E)- NO A (Z) -.
nunca asuma que puede convertir directamente de uno de estos sistemas al otro. Lo único seguro es empezar de cero en cada caso.
¿importa que los dos sistemas a veces den resultados diferentes? ¡No!, El propósito de ambos sistemas es permitirle decodificar un nombre y escribir una fórmula correcta. Si se usan correctamente, ambos sistemas harán esto por usted, aunque el sistema cis-trans solo funcionará para moléculas muy sencillas.
preguntas para probar su comprensión
si este es el primer conjunto de preguntas que ha hecho, lea la página introductoria antes de comenzar. Usted tendrá que utilizar el botón Atrás en su navegador para volver aquí después.,
preguntas sobre la notación E/Z
respuestas
¿a dónde te gustaría ir ahora?
al menú isomerismo. . .
al menú de química orgánica básica. . .
Al Menú Principal . . .