Regole per determinare le priorità
Queste sono note come regole di Cahn-Ingold-Prelog (CIP) dopo le persone che hanno sviluppato il sistema.
La prima regola per casi molto semplici
Guardi prima gli atomi attaccati direttamente agli atomi di carbonio a ciascuna estremità del doppio legame – pensando alle due estremità separatamente.
-
L’atomo che ha il numero atomico più alto ha la priorità più alta.
Diamo un’occhiata all’esempio di cui abbiamo parlato.,

Considera solo il primo isomero e guarda separatamente l’atomo di carbonio sinistro e poi quello destro. Confronta i numeri atomici degli atomi collegati per elaborare le varie priorità.
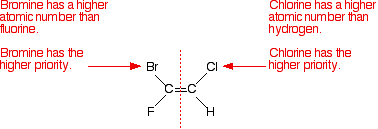
Si noti che gli atomi con le priorità più alte sono entrambi sullo stesso lato del doppio legame. Che conta come (Z)- isomero.
Il secondo isomero ha ovviamente ancora gli stessi atomi ad ogni estremità, ma questa volta gli atomi di priorità più alta si trovano su lati opposti del doppio legame. Questo è l’isomero (E).,
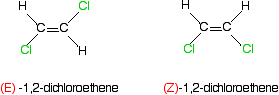
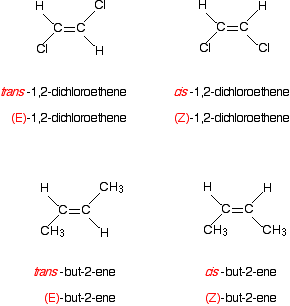
Che dire degli esempi più familiari come 1,2-dicloroetene o but-2-en? Ecco 1,2-dicloroetene.

Pensa alla priorità dei due gruppi sul primo carbonio dell’isomero sinistro.
Il cloro ha un numero atomico più alto dell’idrogeno e quindi ha la priorità più alta. Questo, naturalmente, è altrettanto vero per tutti gli altri atomi di carbonio in questi due isomeri.
Nel primo isomero, i gruppi di priorità più alta si trovano su lati opposti del legame. Questo deve essere l’isomero (E)., L’altro, con i gruppi di priorità più alti sullo stesso lato, è l’isomero (Z).
E ora but-2-en . . .
Questo aggiunge la leggera complicazione che non hai un singolo atomo collegato al doppio legame, ma un gruppo di atomi.
Questo non è un problema. Concentrati sull’atomo direttamente collegato al doppio legame – in questo caso il carbonio nel gruppo CH3. Per questo semplice caso, puoi ignorare completamente gli atomi di idrogeno nel gruppo CH3., Tuttavia, con gruppi più complicati potrebbe essere necessario preoccuparsi di atomi non direttamente collegati al doppio legame. Esamineremo il problema tra un attimo.
Ecco uno degli isomeri di but-2-en:

Il gruppo CH3 ha la priorità più alta perché il suo atomo di carbonio ha un numero atomico di 6 rispetto a un numero atomico di 1 per l’idrogeno anch’esso collegato al doppio legame carbonio-carbonio.
L’isomero disegnato sopra ha i due gruppi di priorità più alti sui lati opposti del doppio legame. Il composto è (E) – but-2-en.,
Un’aggiunta minore alla regola per consentire isotopi di, per esempio, idrogeno
Deuterio è un isotopo di idrogeno avente una massa atomica relativa di 2. Ha ancora solo 1 protone, e quindi ha ancora un numero atomico di 1. Tuttavia, non è lo stesso di un atomo di idrogeno “ordinario”, e quindi questi due composti sono isomeri geometrici:

L’idrogeno e il deuterio hanno lo stesso numero atomico – quindi su quella base, avrebbero la stessa priorità., In un caso del genere, quello con la massa atomica relativa più alta ha la priorità più alta. Quindi in questi isomeri, il deuterio e il cloro sono i gruppi di priorità più alti su ciascuna estremità del doppio legame.
Ciò significa che l’isomero sinistro nell’ultimo diagramma è la forma (E) e quella destra la (Z) -.
Estendere le regole a molecole più complicate
Se stai leggendo questo perché stai facendo un corso per 16 – 18 anni come UK A level, potresti non aver bisogno di sapere molto su questa sezione, ma in realtà non è molto difficile!,
Illustriamo questo prendendo una molecola dall’aspetto abbastanza spaventoso e vedendo quanto sia facile scoprire se si tratta di un isomero (Z) o (E) applicando una regola extra.
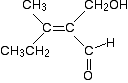
Concentrarsi sull’estremità sinistra della molecola. Cosa è collegato direttamente al doppio legame carbonio-carbonio?
In entrambi i gruppi collegati, un atomo di carbonio è collegato direttamente al legame. Questi due atomi hanno ovviamente lo stesso numero atomico e quindi la stessa priorità. Quindi questo non aiuta.,
In questo tipo di casi, ora si guarda a ciò che è collegato direttamente a quei due carboni (ma senza contare il carbonio del doppio legame) e si confrontano le priorità di questi prossimi lotti di atomi.
Puoi farlo nella tua testa in casi semplici, ma a volte è utile scrivere gli atomi allegati, elencandoli prima con l’atomo di priorità più alta. Li rende più facili da confrontare. Così . . .
Nel gruppo CH3:
Gli atomi attaccati al carbonio sono H H H.
Nel gruppo CH3CH2:
Gli atomi attaccati direttamente al carbonio del gruppo CH2 sono C H H.,
Nel secondo elenco, il C è scritto per primo perché ha il numero atomico più alto.
Ora confronta le due liste atomo per atomo. Il primo atomo in ogni lista è un H nel gruppo CH3 e un C nel gruppo CH3CH2. Il carbonio ha la priorità più alta perché ha il numero atomico più alto. In modo che dà il gruppo CH3CH2 una priorità più alta rispetto al gruppo CH3.
Ora guarda l’altra estremità del doppio legame. La cosa in più che questo illustra è che se si dispone di un doppio legame, si conta l’atomo collegato due volte. Ecco di nuovo la struttura.,

Quindi, di nuovo, gli atomi collegati direttamente al doppio legame carbonio-carbonio sono entrambi carboni. Dobbiamo quindi esaminare cosa è collegato a quei carboni.
Nel gruppo CH2OH:
Gli atomi attaccati direttamente al carbonio sono O H H.
Nel gruppo CHO:
Gli atomi attaccati direttamente al carbonio sono O O H. Ricorda che l’ossigeno viene contato due volte a causa del doppio legame carbonio-ossigeno.
In entrambe le liste, gli ossigeni sono scritti per primi perché hanno un numero atomico più alto dell’idrogeno.,
Quindi, qual è la priorità dei due gruppi? Il primo atomo in entrambe le liste è un ossigeno-che non aiuta. Guarda il prossimo atomo in entrambe le liste. Nel gruppo CH2OH, questo è un idrogeno; nella lista CHO, è un ossigeno.
L’ossigeno ha la priorità più alta – e questo dà al gruppo CHO una priorità più alta rispetto al gruppo CH2OH.
L’isomero è quindi una forma (Z), perché i due gruppi di priorità più alta (il gruppo CH3CH2 e il gruppo CHO) sono entrambi sullo stesso lato del legame.
Questa è stata una spiegazione abbastanza prolissa solo per chiarire come funziona., Con un po ‘ di pratica, ci vogliono pochi secondi per lavorare fuori in qualsiasi, ma i casi più complessi.
Un altro esempio per fare un paio di punti minori aggiuntivi . . .
Ecco una molecola ancora più complicata!
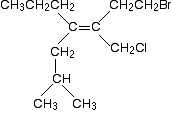
Prima di continuare a leggere, prova a elaborare le priorità relative dei due gruppi all’estremità sinistra del doppio legame e dei due all’estremità destra., C’è un altro po ‘ di regola che non ti ho ancora detto in modo specifico, ma non è difficile indovinare cosa potrebbe essere quando inizi a guardare il problema. Se si può lavorare questo fuori, allora non avrete alcuna difficoltà con qualsiasi problema si rischia di incontrare a questo livello.
Guarda prima i gruppi di sinistra.
In entrambi i gruppi superiore e inferiore, si ha un gruppo CH2 collegato direttamente al doppio legame carbonio-carbonio, e il carbonio in quel gruppo CH2 è anche collegato a un altro atomo di carbonio. In ogni caso, l’elenco leggerà C H H.,
Non c’è differenza tra le priorità di quei gruppi, quindi cosa farai al riguardo? La risposta è spostarsi lungo la catena al gruppo successivo. E se necessario, continua a farlo finché non hai trovato una differenza.
Avanti lungo la catena in alto a sinistra della molecola è un altro gruppo CH2 attaccato ad un ulteriore atomo di carbonio. L’elenco per questo gruppo è di nuovo C H H.
Ma il gruppo successivo lungo la catena in basso a sinistra è un gruppo CH collegato ad altri due atomi di carbonio. La sua lista è quindi C C H.,
Confrontando queste liste atomo per atomo, si porta al fatto che il gruppo inferiore ha la priorità più alta.
Ora guarda i gruppi di destra. Ecco di nuovo la molecola:

Il gruppo in alto a destra ha C H H attaccato al primo carbonio della catena.
Quello in basso a destra ha Cl H H.
Il cloro ha un numero atomico superiore al carbonio, e quindi il gruppo in basso a destra ha la priorità più alta di questi due gruppi.,
Il punto in più che sto cercando di fare con questo bit dell’esempio è che devi solo concentrarti su un bit di una catena alla volta. Non riusciamo mai a considerare il bromo all’estremo in alto a destra della molecola. Non abbiamo bisogno di andare così lontano lungo la catena – si lavora un anello alla volta fino a trovare una differenza. Qualsiasi cosa al di là di questo è irrilevante.
Per la cronaca, questa molecola è a (Z)- isomero perché i gruppi di priorità più alta a ciascuna estremità sono sullo stesso lato del doppio legame.,
Puoi facilmente tradurre cis – e trans – in (Z)- e (E)-?
Potresti pensare che per casi semplici, cis-si convertirà semplicemente in (Z) – e trans-in (E) -.
Guarda ad esempio i casi 1,2-dicloroetene e but-2-en.
Ma non sempre funziona! Pensa a questa molecola relativamente semplice . . .
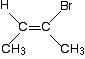
Questo è chiaramente un isomero cis. Ha due gruppi CH3 sullo stesso lato del doppio legame. Ma elaborare le priorità sul lato destro del doppio legame.,
I due atomi direttamente collegati sono carbonio e bromo. Il bromo ha il numero atomico più alto e quindi ha la priorità più alta a tal fine. All’altra estremità, il gruppo CH3 ha la priorità più alta.
Ciò significa che i due gruppi di priorità più alta si trovano su lati opposti del doppio legame, e quindi questo è un (E)- isomero – NON a (Z)-.
Non dare mai per scontato che tu possa convertire direttamente da uno di questi sistemi nell’altro. L’unica cosa sicura da fare è partire da zero in ogni caso.
Importa che i due sistemi a volte diano risultati diversi? No!, Lo scopo di entrambi i sistemi è quello di consentire di decodificare un nome e scrivere una formula corretta. Correttamente utilizzati, entrambi i sistemi lo faranno per te-anche se il sistema cis-trans funzionerà solo per molecole molto semplici.
Domande per testare la tua comprensione
Se questa è la prima serie di domande che hai fatto, leggi la pagina introduttiva prima di iniziare. Sarà necessario utilizzare il pulsante INDIETRO sul browser per tornare qui in seguito.,
domande sulla notazione E / Z
risposte
Dove vorresti andare ora?
Al menu isomerismo. . .
Al menu di chimica organica di base. . .
Al menu principale . . .