zasady określania priorytetów
są one znane jako zasady Cahn-Ingold-Prelog (CIP) od osób, które opracowały system.
pierwsza zasada dla bardzo prostych przypadków
najpierw patrzysz na Atomy przyłączone bezpośrednio do atomów węgla na każdym końcu wiązania podwójnego – myśląc o dwóch końcach osobno.
-
atom, który ma wyższą liczbę atomową, ma wyższy priorytet.
spójrzmy na przykład, o którym mówiliśmy.,

wystarczy wziąć pod uwagę pierwszy izomer – i spojrzeć osobno na lewy, a następnie prawy atom węgla. Porównaj liczby atomowe dołączonych atomów, aby wypracować różne priorytety.
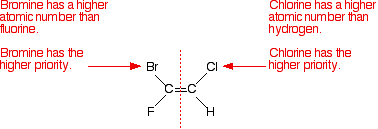
zauważ, że atomy o wyższych priorytetach znajdują się po tej samej stronie wiązania podwójnego. Liczy się jako izomer (Z) -.
drugi izomer oczywiście nadal ma te same Atomy na każdym końcu, ale tym razem Atomy o wyższym priorytecie znajdują się po przeciwnych stronach wiązania podwójnego. To jest (e) – izomer.,
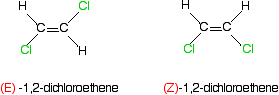
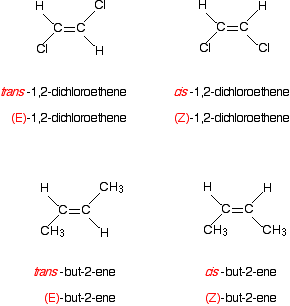
a co z bardziej znanymi przykładami, takimi jak 1,2-dichloroeten lub but-2-en? Oto 1,2-dichloroeten.

chlor ma wyższą liczbę atomową niż wodór, a więc ma wyższy priorytet. To, oczywiście, jest równie prawdziwe dla wszystkich innych atomów węgla w tych dwóch izomerach.
w pierwszym izomerze grupy o wyższym priorytecie znajdują się po przeciwnych stronach wiązania. To musi być izomer (E) -., Drugi, z wyższymi grupami priorytetowymi po tej samej stronie, jest izomerem (Z) -.
i teraz ale-2-ene . . .
dodaje to drobną komplikację, że nie masz pojedynczego atomu przyłączonego do wiązania podwójnego, ale grupę atomów.
to nie problem. Skoncentruj się na atomie bezpośrednio przyłączonym do wiązania podwójnego – w tym przypadku węgla z grupy CH3. W tym prostym przypadku można całkowicie zignorować atomy wodoru w grupie CH3., Jednak w przypadku bardziej skomplikowanych grup może być konieczne martwienie się o Atomy nie przyłączone bezpośrednio do wiązania podwójnego. Za chwilę przyjrzymy się temu problemowi.
oto jeden z izomerów but-2-ENU:

Grupa CH3 ma wyższy priorytet, ponieważ jej atom węgla ma liczbę atomową 6 w porównaniu z liczbą atomową 1 dla wodoru również przyłączonego do podwójnego wiązania węgiel-węgiel.
izomer narysowany powyżej ma dwie wyższe grupy priorytetowe po przeciwnych stronach wiązania podwójnego. Związkiem jest (E) – but-2-en.,
drobny dodatek do zasady pozwalający na izotopy np. wodoru
Deuter jest izotopem wodoru o względnej masie atomowej 2. Nadal ma tylko 1 proton, a więc nadal ma liczbę atomową 1. Jednak nie jest to to samo co atom” zwykłego ” wodoru, więc te dwa związki są izomerami geometrycznymi:

wodór i Deuter mają tę samą liczbę atomową – więc na tej podstawie mają ten sam priorytet., W takim przypadku, ten z wyższą względną masą atomową ma wyższy priorytet. Tak więc w tych izomerach Deuter i chlor są wyższymi grupami priorytetowymi na każdym końcu wiązania podwójnego.
oznacza to, że lewostronny izomer na ostatnim diagramie ma postać (E) -, a prawostronny (Z) -.
Rozszerzanie zasad na bardziej skomplikowane cząsteczki
Jeśli czytasz to, ponieważ robisz kurs dla 16 – 18 latków, takich jak poziom UK a, możesz nie wiedzieć wiele o tej sekcji, ale naprawdę nie jest to bardzo trudne!,
zilustrujmy to, biorąc dość przerażająco wyglądającą cząsteczkę i widząc, jak łatwo jest dowiedzieć się, czy jest to (z)-czy (E) – izomer, stosując dodatkową regułę.
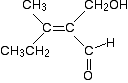
skoncentruj się na lewym końcu cząsteczki. Co jest związane bezpośrednio z podwójnym wiązaniem węgiel-węgiel?
w obu dołączonych grupach atom węgla jest przyłączony bezpośrednio do wiązania. Te dwa atomy oczywiście mają tę samą liczbę atomową, a zatem ten sam priorytet. Więc to nie pomaga.,
w tego typu przypadkach, teraz spojrzeć na to, co jest przyłączone bezpośrednio do tych dwóch atomów (ale bez liczenia węgla wiązania podwójnego) i porównać priorytety tych kolejnych partii atomów.
można to zrobić w głowie w prostych przypadkach, ale czasami warto zapisać dołączone Atomy, wymieniając je najpierw z atomem o najwyższym priorytecie. To sprawia, że łatwiej je porównać. W ten sposób . . .
w grupie CH3:
Atomy przyłączone do węgla to H H.
w grupie CH3CH2:
Atomy przyłączone bezpośrednio do węgla grupy CH2 to C H H.,
na drugiej liście C jest zapisywane jako pierwsze, ponieważ ma najwyższą liczbę atomową.
teraz Porównaj dwie listy atom po atomie. Pierwszy atom na każdej liście to H w grupie CH3 i C w grupie CH3CH2. Węgiel ma wyższy priorytet, ponieważ ma wyższą liczbę atomową. To daje grupie CH3CH2 wyższy priorytet niż grupie CH3.
teraz spójrz na drugi koniec wiązania podwójnego. Dodatkową rzeczą, którą to ilustruje, jest to, że jeśli masz wiązanie podwójne, policzysz dołączony atom dwukrotnie. Oto znowu struktura.,

tak więc, ponownie, Atomy przyłączone bezpośrednio do podwójnego wiązania węgiel-węgiel są zarówno węglami. Musimy zatem przyjrzeć się temu, co jest związane z tymi węglami.
w grupie CH2OH:
Atomy przyłączone bezpośrednio do węgla to O H H.
w grupie CHO:
Atomy przyłączone bezpośrednio do węgla to O O H. pamiętaj, że tlen jest liczony dwukrotnie ze względu na podwójne wiązanie węgiel-tlen.
w obu listach tlenki są zapisywane jako pierwsze, ponieważ mają wyższą liczbę atomową niż wodór.,
więc jaki jest priorytet obu grup? Pierwszy atom na obu listach to tlen – to nie pomaga. Spójrz na Następny atom na obu listach. W grupie CH2OH jest to Wodór; na liście CHO jest to tlen.
tlen ma wyższy priorytet – co daje grupie CHO wyższy priorytet niż grupie CH2OH.
izomer ma zatem postać (Z), ponieważ dwie wyższe grupy priorytetowe (Grupa CH3CH2 i grupa CHO) znajdują się po tej samej stronie wiązania.
To było dość długie Wyjaśnienie, aby wyjaśnić, jak to działa., Z odrobiną praktyki, to trwa kilka sekund, aby wypracować w każdym, ale najbardziej złożonych przypadkach.
jeszcze jeden przykład, aby zrobić kilka dodatkowych drobnych punktów . . .
Oto jeszcze bardziej skomplikowana cząsteczka!
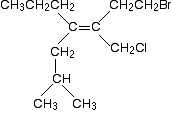
zanim przeczytasz dalej, zapoznaj się z względnymi priorytetami dwóch grup po lewej stronie wiązania podwójnego i dwóch po prawej stronie., Jest jeszcze jedna zasada, której jeszcze Ci nie powiedziałem, ale nietrudno zgadnąć, co to może być, gdy zaczniesz patrzeć na problem. Jeśli możesz to wypracować, nie będziesz miał żadnych trudności z żadnym problemem, który prawdopodobnie natkniesz się na tym poziomie.
Spójrz najpierw na grupy lewostronne.
zarówno w górnej, jak i dolnej grupie, masz grupę CH2 przyłączoną bezpośrednio do podwójnego wiązania węgiel-węgiel, a węgiel w tej grupie CH2 jest również przyłączony do innego atomu węgla. W każdym przypadku lista będzie brzmiała C H H.,
nie ma różnicy między priorytetami tych grup, więc co zamierzasz z tym zrobić? Odpowiedzią jest przejście wzdłuż łańcucha do następnej grupy. A jeśli to konieczne, kontynuuj to, dopóki nie znajdziesz różnicy.
dalej wzdłuż łańcucha w lewym górnym rogu cząsteczki znajduje się kolejna grupa CH2 przyłączona do kolejnego atomu węgla. Lista dla tej grupy to znowu C H H.
ale następna grupa wzdłuż łańcucha w lewym dolnym rogu to grupa CH przyłączona do dwóch kolejnych atomów węgla. Jego lista to C C H.,
porównanie tych list atom po atomie prowadzi do tego, że Dolna Grupa ma wyższy priorytet.
teraz spójrz na grupy prawej strony. Oto znowu cząsteczka:

górna prawa grupa ma c H h przyłączone do pierwszego węgla w łańcuchu.
dolny prawy ma Cl H H.
chlor ma wyższą liczbę atomową niż węgiel, a więc dolna prawa grupa ma wyższy priorytet tych dwóch grup.,
dodatkową kwestią, którą próbuję poruszyć w tym fragmencie przykładu, jest to, że musisz skupić się na jednym kawałku łańcucha na raz. Nigdy nie rozważamy bromu w skrajnym prawym górnym rogu cząsteczki. Nie musimy iść tak daleko wzdłuż łańcucha – ćwiczysz jedno ogniwo na raz, dopóki nie znajdziesz różnicy. Wszystko poza tym jest nieistotne.
dla przypomnienia, cząsteczka ta jest izomerem (Z), ponieważ wyższe grupy priorytetowe na każdym końcu są po tej samej stronie wiązania podwójnego.,
czy można łatwo przetłumaczyć cis – i trans – na (Z)- i (E)-?
można by pomyśleć, że w prostych przypadkach cis-przekształci się w (Z)- i trans – w (E) -.
spójrz na przykład na przypadki 1,2-dichloroetenu i but-2-ENU.
ale to nie zawsze działa! Pomyśl o tej stosunkowo nieskomplikowanej cząsteczce . . .
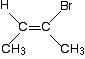
jest to wyraźnie izomer cis. Ma dwie grupy CH3 po tej samej stronie wiązania podwójnego. Ale wypracuj priorytety po prawej stronie podwójnej więzi.,
dwa bezpośrednio przyłączone Atomy to węgiel i brom. Brom ma wyższą liczbę atomową, a więc ma wyższy priorytet na tym końcu. Z drugiej strony grupa CH3 ma wyższy priorytet.
oznacza to, że dwie wyższe grupy priorytetowe znajdują się po przeciwnych stronach wiązania podwójnego, a więc jest to (e) – izomer-a nie (Z) -.
nigdy nie zakładaj, że możesz konwertować bezpośrednio z jednego z tych systemów na drugi. Jedyną bezpieczną rzeczą do zrobienia jest zacząć od zera w każdym przypadku.
czy to ma znaczenie, że te dwa systemy czasami dają różne wyniki? Nie!, Celem obu systemów jest umożliwienie dekodowania nazwy i napisania poprawnej formuły. Właściwie użyte oba systemy zrobią to za ciebie-chociaż system cis-trans będzie działał tylko dla bardzo prostych cząsteczek.
pytania, aby sprawdzić swoje zrozumienie
Jeśli jest to pierwszy zestaw pytań, które zrobiłeś, przeczytaj stronę wprowadzającą przed rozpoczęciem. Musisz użyć przycisku Wstecz w przeglądarce, aby wrócić tutaj później.,
pytania dotyczące notacji E/Z
odpowiedzi
gdzie chciałbyś teraz pojechać?
do menu izomeryzm. . .
do podręcznika podstaw chemii organicznej. . .
do Menu Głównego . . .