Introducción
los injertos de piel de espesor dividido (STSGs) se utilizan rutinariamente para cubrir una variedad de heridas causadas por quemaduras, traumatismos o escisiones tumorales, etc. Debido a su fiabilidad y a la disponibilidad relativamente alta de sitios donantes, los STSG representan una de las primeras opciones en la reconstrucción.,1-3 sin embargo, la recolección de STSGs invariablemente produce una nueva herida abierta en el sitio donante, que puede ser dolorosa y requiere una reepitelización rápida y efectiva.
normalmente, el sitio donante está cubierto con una gasa de malla fina no adherente impregnada con diferentes ungüentos.4,5 Desafortunadamente, esta técnica suele ser dolorosa y es uno de sus principales inconvenientes.6 de hecho, el dolor relacionado con los sitios donantes es la queja más importante del paciente dentro de los primeros diez días después de la cosecha del injerto.7 Esto es particularmente importante en los casos en que se requiere una pronta rehabilitación, p. ej.,, pacientes gravemente quemados.
los recientes avances tecnológicos han hecho posible la creación de nuevos apósitos diseñados para causar menos molestias en las heridas del sitio donante.8,9 a medida que las opciones más nuevas se ven casi a diario, la tendencia actual en el manejo del sitio del donante está orientada a reducir el dolor, así como a promover una reepitelización rápida y efectiva.,10,11
entre los apósitos que se han utilizado en las heridas del sitio donante se encuentran los hidrocoloides (Duoderm®) que típicamente forman una costra sobre la herida y un exudado con un olor desagradable que macera la piel circundante, y Biobrane®, un colágeno porcino tipo I biocompuesto unido a una membrana sintética flexible que ha sido eficaz para reducir el dolor.12 uno de los principales problemas con Biobrane® es que el líquido se acumula debajo si no se usa correctamente, lo que hace que el área sea propensa a la infección.,12
Mepilex® (Mölnlycke Health Care, US, LLC, Norcross, GA) es un apósito de poliuretano no adherente que consiste en una esponja absorbente de poliuretano, adaptable con la tecnología Safetac®. Según los fabricantes, esta tecnología permite que el apósito se adhiera a la piel circundante, pero no al lecho húmedo de la herida, lo que Potencialmente reduce el dolor, previene la maceración y minimiza el arrastre de las células epiteliales en el momento de la extracción.13,14 además, sella la herida para evitar fugas de exudado y aísla la herida del medio ambiente, minimizando las infecciones de la piel.,14
Debido a estas características, es potencialmente beneficioso para STSGs. Realizamos un estudio prospectivo y aleatorizado para evaluar la eficacia de Mepilex® en la reducción del dolor de los sitios donantes de STSG y en la epitelización en comparación con nuestro manejo tradicional (apósito no adherente).
pacientes y métodos
se realizó un ensayo clínico prospectivo, comparativo y aleatorizado entre enero y agosto de 2012. El Comité de Ética de nuestro hospital aprobó el protocolo del estudio. Todos los pacientes incluidos en el estudio firmaron un consentimiento informado., Los criterios de inclusión incluyeron a los pacientes que requerían injertos de piel de espesor dividido secundarios a cualquier etiología. Los pacientes fueron asignados a dos grupos. El primer grupo incluyó a diez pacientes con un sitio donante de al menos 20 cm×10 cm en un muslo. El segundo grupo incluyó cinco pacientes que requirieron cosecha bilateral de STSGs de al menos 10cm×10cm en cada muslo. Los criterios de exclusión incluyeron mujeres embarazadas, pacientes inmunodeprimidos, alergia conocida a cualquier componente de los apósitos, enfermedades dermatológicas y tratamiento anticoagulante o corticosteroide.,
manejo del sitio donante
Todos los injertos de piel fueron recolectados del muslo proximal-anterolateral por el mismo cirujano. Los injertos se recolectaron con un dermatoma para producir un grosor homogéneo de 0,4 mm. en pacientes con un sitio donante unilateral, la herida se dividió en mitades proximal y distal y se asignó aleatoriamente para cubrirse con un apósito no adherente (Adaptic®, Johnson & Johnson, Inc., New Brunswick, NJ), nuestro método estándar, o Mepilex®. El área cubierta con gasa no adherente fue manejada de manera semiabierta, sin vendaje secundario., El parche Mepilex ® fue asegurado con una venda adhesiva (Hypafix®, BSN medical, Inc., Charlotte, NC) y se fue hasta el día 8 (Fig. 1). En los pacientes con sitios donantes bilaterales, un lado fue cubierto con Mepilex® y el otro con Adaptic ® como se describió anteriormente (Fig. 2). Esta asignación se hizo al azar.
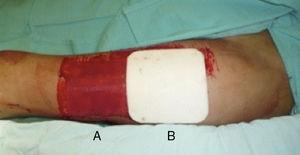
evaluación del sitio donante: (a) área de control cubierta con gasa no adherente, (b) área cubierta con Mepilex®.
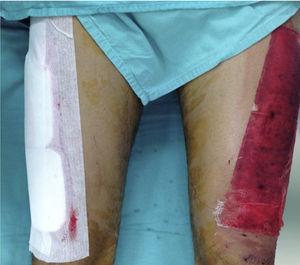
dolor
el dolor de los sitios donantes se evaluó con una escala analógica visual (EVA) utilizando una escala de 0 a 10 los días 3, 5, 7 y 9 después del injerto.,
evaluación de la epitelización
la epitelización se evaluó en los días 8 y 10 en las áreas cubiertas con Mepilex®y en los días 10 en las áreas cubiertas con gasa no adherente. Para retirar la gasa adaptativa, se aplicó una gruesa capa de vaselina sobre el área el 9º día y se dejó durante la noche. A la mañana siguiente se retiró la gasa adaptativa junto a la cama del paciente. Este procedimiento fue indoloro y no se requirió analgésico.
Mepilex® se retiró al 8º día junto a la cama del paciente., Si el área cubierta por Mepilex®no estaba completamente curada al octavo día, se cubrió de nuevo, como se explicó anteriormente para las áreas cubiertas por Mepilex®. Se tomaron fotografías de ambas áreas con una cámara digital (Fuji Finepix S, lente Super EBC Fujinon: zoom óptico 26× f=4.3–111.8, 1:3.1–5.9) usando ajustes fotográficos estandarizados (distancia de 30 cm, f30, 1/30 e ISO 100) bajo lámparas fluorescentes de luz diurna estándar (lámpara fluorescente lineal estándar GE T8 36W, 2750lm).
Las fotografías fueron evaluadas por un cirujano plástico ciego al grupo y al punto de tiempo después del injerto., El porcentaje de epitelización se calculó analizando las fotografías de los sitios donantes utilizando el software de imagen (Adobe Photoshop®). Brevemente, se seleccionó el área del sitio donante y se determinó la cantidad de píxeles dentro de la selección. Luego, se seleccionaron las áreas no selladas y se determinó el tamaño respectivo de esta selección. El porcentaje de epitelización se calculó dividiendo el área no epitelizada por la superficie total del sitio donante (Fig. 3a y b).
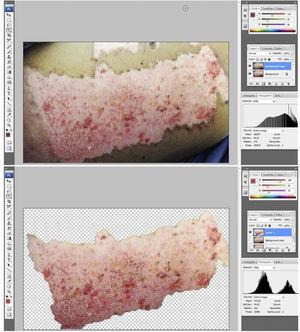
análisis Estadístico
la Diferencia en las puntuaciones de la escala analógica visual se evaluó mediante análisis de VARIANZA de Rangos. La diferencia de áreas epitelizadas se evaluó con ANOVA unidireccional (Sigma Stat 3.5, Alemania)., La significancia fue definida como p
0,05.Resultados se incluyeron
quince pacientes que requirieron injerto de piel para el manejo de lesiones traumáticas (Fig. 4). Había 11 hombres y 4 mujeres con una mediana de edad de 27 años (rango 10-68) (Tabla 1).

algoritmo de estudio.
etiología de la herida y características del paciente.,
| Etiology | n |
|---|---|
| Trauma | 9 |
| Burn | 4 |
| Tumor resection | 2 |
| Gender | |
| Male | 11 |
| Female | 4 |
| Age, yrs., la mediana (rango) | 27 (10-68) |
Postoperatorio sitio donante dolor fue consistentemente menor en las áreas cubiertas con Mepilex durante el estudio. Las puntuaciones medias de dolor para todo el período de tratamiento fueron de 6,07±1,46 para el control y de 1,72±1,6 para Mepilex®. El análisis de cada punto de tiempo mostró resultados similares: en el tercer día, los pacientes reportaron una puntuación media EVA de 3,4±1,3 para el grupo Mepilex® y 7,07±1,16 para el grupo control; en el quinto día 1,87±1.,55 en el grupo Mepilex® y 6.33±1.4 en el grupo control; en el día siete 0.93±1.03 en el grupo Mepilex® y 5.8±1.21 en el grupo control, y en el día nueve 0.67±0.82 en el grupo Mepilex® y 5.07±1.39 en el grupo control (p
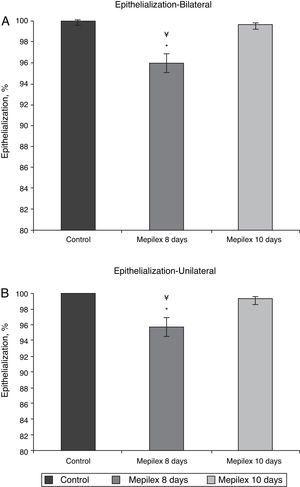
0.001) (Fig. 5). El análisis posterior reveló resultados similares en los pacientes con tratamiento unilateral (tanto para Mepilex® como Adaptic en el mismo muslo) y los tratados bilateralmente (Mepilex® en un muslo y Adaptic en el contralateral) (P0.001) (Fig. 6a y b).

evaluación general del dolor. Las puntuaciones de dolor fueron consistentemente más bajas en el grupo de Mepilex en todo momento durante el estudio. * p0. 001(ver texto para más detalles). VAS: escala analógica visual.
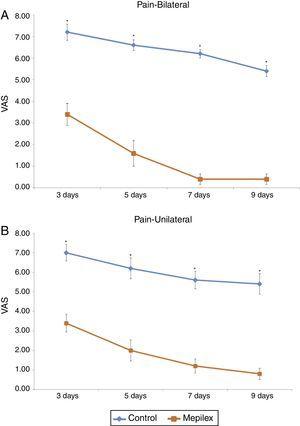
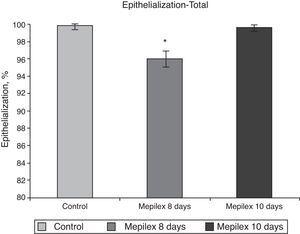
General epithelialization assessment. Areas covered with Mepilex were partially epithelialized at day 8 (95.94%,) significantly different that control and Mepilex at day 10 (p=0.008). At day 10, no significant difference was observed.
Discusión
La elección del apósito para el sitio donante puede tener un gran impacto en la satisfacción del paciente y la recuperación.15 la recolección de injertos de piel resulta en grandes áreas de superficie abiertas que son propensas al dolor, infección u otras morbilidades.16,17 el manejo del sitio donante juega un papel importante y crítico en la evolución y Rehabilitación de los pacientes porque la rehabilitación y movilización tempranas son críticas para lograr resultados óptimos en pacientes quemados.,18,19
el dolor perjudica la pronta rehabilitación, ya que el dolor relacionado con los sitios donantes es la queja más importante dentro de los primeros diez días después de la recolección del injerto en pacientes quemados.7 por lo tanto, al disminuir el dolor, podríamos ayudar potencialmente a la movilización temprana de los pacientes, especialmente en poblaciones pediátricas.
todos los tipos de apósitos están reportados en la literatura para el manejo del sitio donante, pero todos tienen diferentes inconvenientes y el apósito ideal aún no ha sido descrito.,20,21 en nuestra continua búsqueda del material disponible que mejor se adapte a las necesidades de nuestros pacientes quemados, decidimos evaluar Mepilex® por su potencial ventaja de reducción del dolor sin afectar el epitelio. El objetivo principal de nuestro estudio fue evaluar la reducción del dolor en los sitios donantes. Dado que el dolor es un parámetro subjetivo y varía de individuo a individuo, es muy difícil hacer mediciones objetivas y confiables.22 por lo tanto, se utilizó la EVA, que es una herramienta ampliamente utilizada y aceptada para la evaluación del dolor.,15,23
las áreas donantes se ubicaron en el muslo anterolateral en todos los casos para reducir la variabilidad del dolor relacionado con el área topográfica. Se decidió incluir pacientes con sitios donantes unilaterales y bilaterales para comparar el efecto del apósito en la reducción del dolor, ya que ambos enfoques tienen sus pros y sus contras. En ambos casos, el paciente sirve como su propio control, lo que es deseable ya que el uso de diferentes pacientes para grupos de control y tratamiento hace que la eliminación del efecto psicológico de cada individuo sobre la percepción del dolor sea muy difícil, aumentando el sesgo del estudio., Dividiendo los sitios donantes en mitades (proximal y distal) estamos evaluando la misma área anatómica, disminuyendo la variabilidad para un área topográfica diferente. A pesar de que existe una posibilidad razonable de mala discriminación del dolor entre zonas adyacentes, los puntajes fueron significativamente diferentes en ambas áreas, confirmando que el paciente es capaz de discriminar el dolor en dos áreas adyacentes. El tratamiento bilateral permitió eliminar la dificultad teórica de discriminar efectivamente el dolor en dos áreas adyacentes, pero incluye el sesgo de dos áreas topográficas., Sin embargo, dado que el dolor se redujo efectivamente con Mepilex® en ambos casos, podemos afirmar su superioridad sobre el manejo estándar en la reducción del dolor.
generalmente retiramos la gasa no adherente de los sitios donantes en el día 10 porque hemos encontrado que la epitelización está completa para ese momento, y los intentos anteriores de eliminar la gasa antes llevaron casi invariablemente a heridas sin cicatrizar. Por lo tanto, decidimos quitar los apósitos ese día y elegirlo como el último punto de tiempo para la comparación.,
dado que la epitelización se completó prácticamente en ambos grupos al día 10 y esto no fue estadísticamente diferente (p=0.29), podemos concluir que Mepilex® no perjudica la epitelización de los sitios donantes. Decidimos retirar Mepilex® antes del día 10 porque queríamos ver si mejoraría la epitelización. Se decidió arbitrariamente fijar el día 8 para evaluar la epitelización en el grupo de Mepilex®, ya que si realmente mejorara la epitelización, esto sería clínicamente relevante., Dado que la epitelización fue incompleta estadística y clínicamente relevante para el día 8, no recomendamos la eliminación en ese día. Se necesitaría un nuevo estudio para evaluar si Mepilex® puede inducir la epitelización completa para el día 9, pero creemos que esto es poco probable y clínicamente irrelevante. Una excepción para esto sería en pacientes gravemente quemados que típicamente requieren varias tomas de injerto y un día ahorrado con cada cosecha sería ventajoso.
aunque el tamaño muestral es relativamente pequeño (15 pacientes), se logró significación estadística y potencia (p
0,001, potencia 1,00)., Por lo tanto, no creemos que el aumento del tamaño de la muestra influya en el resultado. Otra limitación de este estudio es el hecho de que el paciente no estaba ciego al tratamiento y es difícil eliminar el efecto placebo. No fue posible obtener material de vendaje sin la tecnología Safetac. Tal vez estudios futuros puedan comparar otro material de apósito oclusivo para determinar si este tipo de tecnología es responsable de la reducción del dolor observada o del método oclusivo per se.,
sin embargo, encontramos que Mepilex® era un apósito fácil de usar, indoloro en el momento de la extracción, y mantuvo su posición durante todo el período de tratamiento, lo que no siempre es posible con otros materiales de apósito; por ejemplo, hidrocoloides. Otra ventaja fue que en este tipo de heridas moderadamente exudantes, Mepilex ® absorbió eficientemente los exudados sin necesidad de vendajes secundarios. No fue necesario cambiar el parche debido a la saturación de líquido en ningún momento., El hecho de que no haya deterioro en la tasa de epitelización en el sitio donante cubierto alienta su uso en casos en los que se requiere que el área donante esté en contacto con la cama; por ejemplo, muslo posterior o pacientes en posición prona. Es bien sabido que esta práctica puede complicar estas áreas con el manejo convencional. No hubo informes de efectos adversos con el uso de Mepilex® en ningún paciente y prefirieron el uso de Mepilex® en lugar del tratamiento estándar en todos los casos.,
por lo tanto, podemos concluir que el uso de Mepilex® se traduce en una reducción significativa y relevante del dolor en sitios donantes sin afectar la epitelización.
divulgación
los autores declaran que no han publicado ningún manuscrito similar a este estudio que pueda ser considerado como trabajo redundante o duplicado.
financiación
no se prestó apoyo financiero.
conflicto de intereses
los autores no tienen conflictos de intereses que declarar.