Introduzione
Gli innesti cutanei a spessore diviso (STSGs) vengono abitualmente utilizzati per coprire una varietà di ferite causate da ustioni, traumi o escisioni tumorali, ecc. Grazie alla loro affidabilità e alla disponibilità relativamente elevata di siti donatori, gli STSG rappresentano una delle prime opzioni nella ricostruzione.,1-3 Tuttavia, la raccolta di STSGS produce invariabilmente una nuova ferita aperta nel sito donatore, che può essere dolorosa e richiede una riepitelizzazione rapida ed efficace.
Tipicamente, il sito donatore è coperto con garza a maglia fine non aderente impregnata con diversi unguenti.4,5 Sfortunatamente, questa tecnica è solitamente dolorosa ed è uno dei suoi principali inconvenienti.6 Infatti, il dolore legato ai siti donatori è la lamentela più importante del paziente entro i primi dieci giorni dopo il raccolto dell’innesto.7 Ciò è particolarmente importante nei casi in cui è necessaria una pronta riabilitazione, ad es.,, pazienti gravemente ustionati.
I recenti progressi tecnologici hanno reso possibile la creazione di nuove medicazioni progettate per causare meno disagio nelle ferite del sito donatore.8,9 Poiché le nuove opzioni sono viste quasi quotidianamente, l’attuale tendenza nella gestione del sito donatore è orientata a ridurre il dolore e promuovere una riepitelizzazione rapida ed efficace.,10,11
Tra le medicazioni che sono state utilizzate nelle ferite del sito donatore ci sono gli idrocolloidi (Duoderm®) che tipicamente formano una crosta sulla ferita e un essudato con un odore sgradevole che macera la pelle circostante, e Biobrane®, un collagene biocomposito di tipo I suino collegato a una membrana sintetica flessibile che è stata efficace nel ridurre il dolore.12 Uno dei problemi principali con Biobrane® è che il liquido si accumula al di sotto se non utilizzato correttamente, rendendo l’area soggetta a infezioni.,12
Mepilex® (Mölnlycke Health Care, US, LLC, Norcross, GA) è una medicazione poliuretanica non aderente costituita da una spugna poliuretanica assorbente, adattabile con Safetac Technology®. Secondo i produttori, questa tecnologia consente alla medicazione di aderire alla pelle circostante, ma non al letto della ferita umida, riducendo potenzialmente il dolore, prevenendo la macerazione e riducendo al minimo il trascinamento delle cellule epiteliali alla rimozione.13,14 Inoltre, sigilla la ferita per evitare perdite di essudato e isola la ferita dall’ambiente, riducendo al minimo le infezioni cutanee.,14
A causa di queste caratteristiche, è potenzialmente vantaggioso per STSGs. Abbiamo condotto uno studio prospettico e randomizzato per valutare l’efficacia di Mepilex® nella riduzione del dolore dei siti donatori di STSG e sull’epitelizzazione rispetto alla nostra gestione tradizionale (medicazione non aderente).
Pazienti e metodi
Abbiamo condotto uno studio clinico prospettico, comparativo e randomizzato tra gennaio e agosto 2012. Il Comitato Etico del nostro ospedale ha approvato il protocollo di studio. Tutti i pazienti arruolati nello studio hanno firmato un consenso informato., I criteri di inclusione includevano pazienti che richiedevano innesti cutanei a spessore diviso secondari a qualsiasi eziologia. I pazienti sono stati assegnati a due gruppi. Il primo gruppo comprendeva dieci pazienti con un sito donatore di almeno 20 cm×10 cm su una coscia. Il secondo gruppo comprendeva cinque pazienti che richiedevano un raccolto bilaterale di STSGS di almeno 10 cm×10 cm su ciascuna coscia. I criteri di esclusione includevano donne in gravidanza, pazienti immunosoppressi, allergia nota a qualsiasi componente delle medicazioni, malattie dermatologiche e trattamento anticoagulante o corticosteroide.,
Gestione del sito del donatore
Tutti gli innesti cutanei sono stati prelevati dalla coscia prossimale-anterolaterale dallo stesso chirurgo. Gli innesti sono stati raccolti con un dermatoma per produrre uno spessore omogeneo di 0,4 mm. Nei pazienti con un sito donatore unilaterale, la ferita è stata divisa in metà prossimale e distale e assegnata casualmente per essere coperta con una medicazione non aderente (Adaptic®, Johnson & Johnson, Inc., New Brunswick, NJ), il nostro metodo standard, o Mepilex®. L’area coperta con garza non aderente è stata gestita in modo semiaperto, senza medicazione secondaria., Il cerotto Mepilex ® è stato fissato con una benda adesiva (Hypafix®, BSN medical, Inc., Charlotte, NC) e lasciato sul posto fino all ‘ 8 ° giorno (Fig. 1). Nei pazienti con siti donatori bilaterali, un lato è stato coperto con Mepilex® e l’altro con Adaptic® come descritto in precedenza (Fig. 2). Questo incarico è stato fatto in modo casuale.
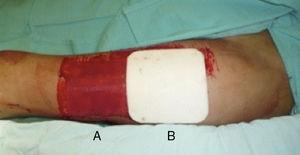
Valutazione del sito del donatore: (a) area di controllo coperta con garza non aderente, (b) Area coperta da Mepilex®.
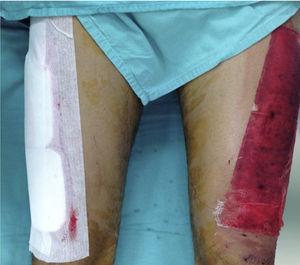
Paziente con sito donatore bilaterale: un lato è stato coperto con Mepilex (a destra) e il lato controlaterale (a sinistra) con garza non aderente.
Dolore
Il dolore dei siti donatori è stato valutato con una scala analogica visiva (VAS) utilizzando una scala da 0 a 10 nei giorni 3, 5, 7 e 9 dopo l’innesto.,
Valutazione dell’epitelizzazione
L’epitelizzazione è stata valutata l ‘ 8 ° e il 10 ° giorno nelle aree coperte da Mepilex®e il 10 ° giorno nelle aree coperte con garza non aderente. Per rimuovere la garza adattica, uno spesso strato di vaselina è stato applicato sull’area il 9 ° giorno e lasciato durante la notte. La mattina dopo la garza adattica è stata rimossa al capezzale del paziente. Questa procedura è stata indolore e non è stato richiesto alcun analgesico.
Mepilex® è stato rimosso l ‘ 8 ° giorno al capezzale del paziente., Se l’area coperta da Mepilex®non è stata completamente guarita entro l ‘ 8 ° giorno, è stata nuovamente coperta, come precedentemente spiegato per le aree coperte da Mepilex®. Le fotografie sono state scattate di entrambe le aree con una fotocamera digitale (Fuji Finepix S, Super EBC Fujinon obiettivo: 26× zoom ottico f=4.3–111.8, 1:3.1–5.9) utilizzo di impostazioni foto standardizzate (distanza 30 cm, f30, 1/30 e ISO 100) sotto lampade fluorescenti a luce diurna standard (lampada fluorescente lineare standard GE T8 36W, 2750lm).
Le fotografie sono state valutate da un chirurgo plastico accecato al gruppo e al punto temporale dopo l’innesto., La percentuale di epitelizzazione è stata calcolata analizzando le fotografie dei siti donatori utilizzando il software di immagine (Adobe Photoshop®). In breve, è stata selezionata l’area del sito donatore e determinata la quantità di pixel all’interno della selezione. Quindi, le aree non cicatrizzate sono state selezionate e la rispettiva dimensione di questa selezione è stata determinata. La percentuale di epitelizzazione è stata calcolata dividendo l’area non epitelizzata per l’area totale del sito donatore (Fig. 3 bis e b).
Valutazione del sito del donatore: (a) area del sito del donatore da valutare. Il chirurgo che valuta il tasso di epitelizzazione è stato accecato al gruppo e al punto temporale dell’area; (b) l’estensione (in pixel) dell’area non guarita è stata determinata dividendo l’area non guarita sull’area totale del sito donatore.
Analisi statistica
La differenza nei punteggi della scala analogica visiva è stata valutata da ANOVA sui ranghi. La differenza delle aree epitelizzate è stata valutata con ANOVA a senso unico (Sigma Stat 3.5, Germania)., Il significato è stato definito come p
0.05.Risultati
Sono stati inclusi quindici pazienti che hanno richiesto l’innesto cutaneo per la gestione delle lesioni traumatiche (Fig. 4). C’erano 11 uomini e 4 donne con un’età media di 27 anni (intervallo 10-68) (Tabella 1).
Algoritmo di studio.
Eziologia della ferita e caratteristiche del paziente.,
| Etiology | n |
|---|---|
| Trauma | 9 |
| Burn | 4 |
| Tumor resection | 2 |
| Gender | |
| Male | 11 |
| Female | 4 |
| Age, yrs., mediana (range) | 27 (10-68) |
Postoperatorio sito donatore dolore è stato costantemente inferiore nelle aree coperte con Mepilex® durante lo studio. I punteggi medi del dolore per l’intero periodo di trattamento sono stati 6,07±1,46 per il controllo e 1,72±1,6 per Mepilex®. L’analisi di ogni punto temporale ha mostrato risultati simili: al terzo giorno, i pazienti hanno riportato un punteggio VAS medio di 3,4±1,3 per il gruppo Mepilex® e 7,07±1,16 per il gruppo di controllo; al quinto giorno 1,87±1.,55 nel gruppo Mepilex® e 6,33±1,4 nel gruppo di controllo; al settimo giorno 0,93±1,03 nel gruppo Mepilex® e 5,8±1,21 nel gruppo di controllo e al nono giorno 0,67±0,82 nel gruppo Mepilex® e 5,07±1,39 nel gruppo di controllo (p
0,001) (Fig. 5). Ulteriori analisi hanno rivelato risultati simili nei pazienti con trattamento unilaterale (sia per Mepilex® che per Adaptic sulla stessa coscia) e in quelli trattati bilateralmente (Mepilex® su una coscia e Adaptic su quella controlaterale) (p0.001) (Fig. 6 bis e b).

Valutazione generale del dolore. I punteggi del dolore sono stati costantemente inferiori nel gruppo trattato con Mepilex in ogni momento dello studio. * p0.001 (vedi testo per i dettagli). VAS: scala analogica visiva.
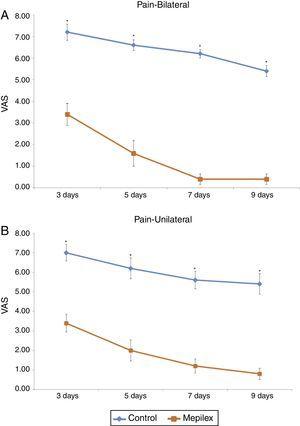
Valutazione del dolore per gruppi. L’analisi dei gruppi ha mostrato significativamente meno dolore nelle aree coperte con Mepilex® in tutti i punti temporali (p0.01). a) Siti donatori bilaterali. b) Siti donatori unilaterali. VAS: scala analogica visiva.,
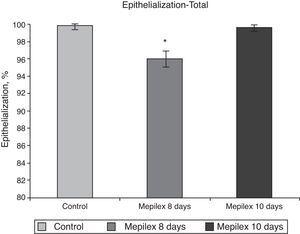
General epithelialization assessment. Areas covered with Mepilex were partially epithelialized at day 8 (95.94%,) significantly different that control and Mepilex at day 10 (p=0.008). At day 10, no significant difference was observed.
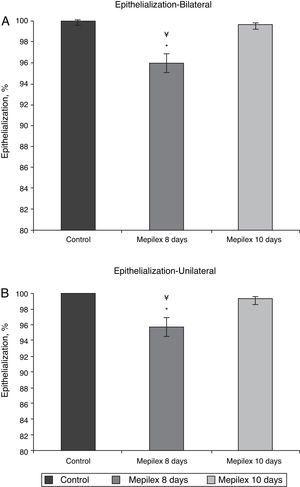
Valutazione dell’epitelizzazione per gruppi. Le aree coperte con Mepilex erano significativamente meno epitelizzate al giorno 8 rispetto al giorno 10 in entrambi i gruppi. A) Siti donatori bilaterali. (B) Siti donatori unilaterali (vedi testo per i dettagli). * p = 0,003 vs. Mepilex 10 giorni. ¥p0. 001 vs. controllo
Discussione
La scelta della medicazione per il sito donatore può avere un impatto importante sulla soddisfazione e sul recupero del paziente.15 La raccolta dell’innesto cutaneo si traduce in ampie superfici aperte soggette a dolore, infezione o altre morbosità.16,17 La gestione del sito donatore svolge un ruolo importante e critico nell’evoluzione e nella riabilitazione dei pazienti perché la riabilitazione precoce e la mobilitazione sono fondamentali per ottenere risultati ottimali nei pazienti ustionati.,18,19
Il dolore compromette la pronta riabilitazione, poiché il dolore correlato ai siti donatori è la lamentela più importante entro i primi dieci giorni dopo la raccolta del trapianto nei pazienti ustionati.7 Pertanto, diminuendo il dolore, potremmo potenzialmente aiutare la mobilitazione precoce dei pazienti, specialmente nelle popolazioni pediatriche.
Tutti i tipi di medicazioni sono riportati in letteratura per la gestione del sito donatore, ma hanno tutti diversi inconvenienti e la medicazione ideale deve ancora essere descritta.,20,21 Nella nostra continua ricerca del materiale disponibile che meglio si adatta alle esigenze dei nostri pazienti ustionati, abbiamo deciso di valutare Mepilex® per il suo potenziale vantaggio di riduzione del dolore senza intaccare l’epitelio. Lo scopo principale del nostro studio era quello di valutare la riduzione del dolore dei siti donatori. Poiché il dolore è un parametro soggettivo e varia da individuo a individuo, è molto difficile effettuare misurazioni oggettive e affidabili.22 Pertanto, abbiamo utilizzato il VAS, che è uno strumento ampiamente utilizzato e accettato per la valutazione del dolore.,15,23
Aree donatrici sono state localizzate nella coscia anterolaterale in tutti i casi per ridurre la variabilità del dolore correlato all’area topografica. Abbiamo deciso di includere pazienti con siti donatori unilaterali e bilaterali per confrontare l’effetto della medicazione nel ridurre il dolore perché entrambi gli approcci hanno i suoi pro e contro. In entrambi i casi, il paziente funge da proprio controllo, il che è auspicabile poiché l’utilizzo di diversi pazienti per gruppi di controllo e trattamento rende molto difficile l’eliminazione dell’effetto psicologico di ogni individuo sulla percezione del dolore, aumentando il pregiudizio dello studio., Dividendo i siti donatori in metà (prossimale e distale) stiamo valutando la stessa area anatomica, diminuendo la variabilità per una diversa area topografica. Anche se esiste una ragionevole possibilità di scarsa discriminazione del dolore tra le zone adiacenti, i punteggi erano significativamente diversi in entrambe le aree, confermando che il paziente è in grado di discriminare il dolore in due aree adiacenti. Il trattamento bilaterale ha permesso di rimuovere la difficoltà teorica di discriminare efficacemente il dolore in due aree adiacenti, ma include il bias di due aree topografiche., Tuttavia, poiché il dolore è stato efficacemente ridotto con Mepilex® in entrambi i casi, possiamo affermare la sua superiorità rispetto alla gestione standard nella riduzione del dolore.
Di solito rimuoviamo la garza non aderente dei siti donatori al giorno 10 perché abbiamo scoperto che l’epitelizzazione è completa a quel punto, e precedenti tentativi di rimuovere la garza in precedenza hanno portato quasi invariabilmente a ferite non cicatrizzate. Pertanto, abbiamo deciso di rimuovere le medicazioni in quel giorno e l’abbiamo scelto come punto temporale finale per il confronto.,
Poiché l’epitelizzazione è stata praticamente completata in entrambi i gruppi entro il giorno 10 e questo non era statisticamente diverso (p=0,29), possiamo concludere che Mepilex® non compromette l’epitelizzazione dei siti donatori. Abbiamo deciso di rimuovere Mepilex® prima del 10 ° giorno perché volevamo vedere se avrebbe migliorato l’epitelizzazione. È stato arbitrariamente deciso di impostare il giorno 8 per valutare l’epitelizzazione nel gruppo Mepilex®, perché se effettivamente migliorasse l’epitelizzazione, questo sarebbe clinicamente rilevante., Poiché l’epitelizzazione era statisticamente e clinicamente rilevante incompleta entro il giorno 8, non consigliamo la rimozione in quel giorno. Sarebbe necessario un nuovo studio per valutare se Mepilex® può indurre una completa epitelizzazione entro il giorno 9, ma riteniamo che ciò sia improbabile e clinicamente irrilevante. Un’eccezione per questo sarebbe in pazienti gravemente bruciati che in genere richiedono diversi innesto prende e un giorno salvato con ogni raccolto sarebbe vantaggioso.
Anche se la dimensione del campione è relativamente piccola (15 pazienti), la significatività statistica e la potenza sono state raggiunte (p
0,001, potenza 1,00)., Pertanto, non crediamo che l’aumento della dimensione del campione influenzerebbe il risultato. Un’altra limitazione di questo studio è il fatto che il paziente non è stato accecato al trattamento ed è difficile eliminare l’effetto placebo. Non è stato possibile ottenere materiale di medicazione senza la tecnologia Safetac. Forse studi futuri possono confrontare altri materiali di medicazione occlusiva per determinare se questo tipo di tecnologia è responsabile della riduzione del dolore osservata o del metodo occlusivo di per sé.,
Tuttavia, abbiamo scoperto che Mepilex® era una medicazione facile da usare, indolore alla rimozione, e ha mantenuto la sua posizione durante l’intero periodo di trattamento, cosa che non è sempre possibile con altri materiali di medicazione; ad esempio, idrocolloidi. Un altro vantaggio era che in questo tipo di ferita moderatamente essudante, Mepilex® assorbiva efficacemente gli essudati senza la necessità di medicazioni secondarie. Non è stato necessario cambiare il cerotto a causa della saturazione del fluido in qualsiasi momento., Il fatto che non vi sia stata alcuna compromissione del tasso di epitelizzazione nel sito donatore coperto incoraggia il suo uso nei casi in cui l’area donatrice deve essere in contatto con il letto; ad esempio, coscia posteriore o pazienti in posizione prona. È noto che questa pratica può complicare queste aree con la gestione convenzionale. Non ci sono state segnalazioni di effetti avversi con l’uso di Mepilex® in nessun paziente e hanno preferito l’uso di medicazione Mepilex® invece della gestione standard in tutti i casi.,
Pertanto, possiamo concludere che l’uso di Mepilex® si traduce in una significativa e rilevante riduzione del dolore nei siti donatori senza influenzare l’epitelizzazione.
Disclosure
Gli autori dichiarano di non aver pubblicato alcun manoscritto simile a questo studio che possa essere considerato un lavoro ridondante o duplicato.
Finanziamento
Non è stato fornito alcun sostegno finanziario.
Conflitto di interessi
Gli autori non hanno conflitti di interesse da dichiarare.