l’uvéite antérieure aiguë associée à HLA-B27 est le type d’uvéite endogène le plus fréquent (voir image ci-dessous), représentant 18 à 32% de tous les cas d’uvéite antérieure dans les pays occidentaux et 6 à 13% de tous les cas D’uvéite antérieure en Asie. La fréquence relativement plus faible en Asie est liée à la fréquence plus faible de HLA-B27 trouvée dans cette population., Comme nous l’avons mentionné, il existe différents modèles globaux d’AUA associées à HLA-B27 qui peuvent être attribués à différents facteurs génétiques, tels que les polymorphismes HLA-B27 et les gènes non MHC. Ces variations géographiques peuvent également exister en raison de facteurs environnementaux pathogènes encore non identifiés.
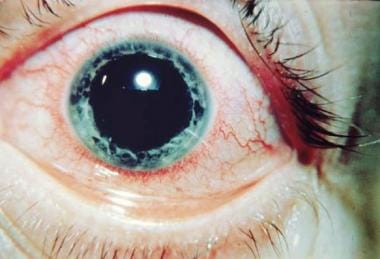 uvéite antérieure Aiguë dans la spondylarthrite ankylosante. Avec L’aimable autorisation de Paul Dieppe, BSc, MD, FRCP, FFPHM.,
uvéite antérieure Aiguë dans la spondylarthrite ankylosante. Avec L’aimable autorisation de Paul Dieppe, BSc, MD, FRCP, FFPHM., des études indiquent que L’uvéite associée à HLA-B27 est une entité distincte caractérisée par une prédominance masculine et une association fréquente avec des syndromes arthritiques séronégatifs, tels que la spondylarthrite ankylosante, l’arthrite réactive, l’arthrite psoriasique et les maladies inflammatoires de l’intestin. Le premier épisode d’AUA associée à HLA-B27 survient le plus souvent chez les patients âgés de 20 à 40 ans, alors que l’âge d’apparition de L’AUA négative à HLA-B27 a tendance à se produire une décennie plus tard. Parmi les patients atteints D’AUA, 50 à 60% peuvent être positifs au HLA-B27., Il s’agit généralement d’une maladie unilatérale bénigne Non granulomateuse se présentant comme une triade classique de douleur, de rougeur et de photophobie.
Les manifestations cornéennes peuvent inclure de fins précipités kératitiques et de la fibrine sur l’endothélium. L’œdème cornéen peut résulter d’un compromis endothélial et d’une décompensation. La kératopathie en bande, une accumulation de calcium dans l’épithélium cornéen, peut être observée dans l’uvéite chronique., La chambre antérieure montre des cellules et une fusée éclairante, qui est une brume observée lors de l’examen à la lampe à fente, reflétant l’accumulation de protéines dans la chambre antérieure due à la dégradation de la barrière hémato-aqueuse, et, en cas d’inflammation sévère, l’exsudat fibrineux dans la chambre antérieure peut obstruer la pupille, provoquant une bombe Cette fibrine peut être confondue avec une endophtalmie endogène, une cataracte ou une hypopyon. Un hypopyon peut être vu, et, rarement, même un hyphème spontané se produit à la suite de vaisseaux iris sévèrement dilatés.,
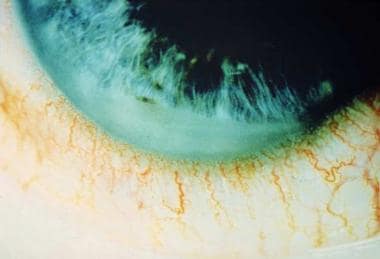 chambre Antérieure de fibrine collection dans la spondylarthrite ankylosante. Avec L’aimable autorisation de Paul Dieppe, BSc, MD, FRCP, FFPHM.
chambre Antérieure de fibrine collection dans la spondylarthrite ankylosante. Avec L’aimable autorisation de Paul Dieppe, BSc, MD, FRCP, FFPHM. une dispersion pigmentaire, un myosis pupillaire et des nodules de l’iris peuvent être notés, et des synéchies, antérieures et postérieures, peuvent survenir. L’atteinte du segment postérieur est relativement rare, mais un œdème maculaire cystoïde, un œdème discal, des exsudats pars plana ou une choroïdite peuvent être observés. La pression intraoculaire est souvent faible, secondaire à une diminution de la production aqueuse avec inflammation du corps ciliaire et maillage trabéculaire., La pression intraoculaire peut également être élevée si les cellules inflammatoires et les débris obstruent le maillage trabéculaire, en particulier chez les patients présentant une mauvaise facilité de sortie préexistante.
L’AUA suit généralement une courte cure de quelques jours à quelques semaines jusqu’à 3 mois, avec une tendance à se reproduire dans le même œil, en particulier chez les personnes positives à HLA-B27. Les Complications de L’AUA comprennent la cataracte, le glaucome, l’hypotonie, l’œdème maculaire cystoïde et la formation de synéchies., Le pronostic de l’uvéite antérieure associée à HLA-B27, avec ou sans maladie systémique, est moins favorable par rapport aux patients qui sont HLA-B27 négatifs avec uvéite antérieure idiopathique. Malgré le potentiel de séquelles, le pronostic global est bon.
L’AUA classique se résout complètement lorsqu’elle est traitée rapidement et agressivement. Les cas sous-traités ou mal diagnostiqués peuvent évoluer vers une iridocyclite chronique en raison de dommages permanents de la barrière hémato-aqueuse.,
diagnostic
Une histoire minutieuse et un examen physique aident habituellement à distinguer entre les entités uvéitiques associées à la maladie systémique et HLA-B27 de celles qui ne sont pas associées à HLA-B27. Les entités pathologiques causant L’AUA sont variées et comprennent l’iritis traumatique, l’iritis d’extraction postcataracte, la polyarthrite rhumatoïde juvénile, l’infection herpétique (herpès simplex et herpès zoster), la syphilis, la sarcoïdose, L’iridocyclite Hétérochromique de Fuchs, la crise glaucomatocyclitique, la maladie de Behcet et l’endophtalmie de bas grade.,
le rôle du test HLA-B27 chez les patients atteints d’AUA unilatérale est important dans le diagnostic différentiel. L’absence D’antigène HLA-B27 dans l’AUA unilatérale peut être un indice pour le clinicien de rechercher d’autres entités d’uvéite spécifiques et d’autres maladies systémiques. Il peut également être utile pour déterminer le pronostic de L’AUA, car l’AUA associée à HLA-B27, même en l’absence de maladie systémique, est moins favorable et plus susceptible de se reproduire par rapport à celle des patients qui sont HLA-B27 négatifs.,
traitement
la prise en charge médicale de L’AUA comprend les corticostéroïdes topiques ou systémiques et les cycloplégiques topiques. Les injections de corticostéroïdes périoculaires sont extrêmement utiles dans les cas aigus, récalcitrants ou non conformes, en particulier lorsque l’atteinte du segment postérieur se produit. Un traitement immunosuppresseur peut être nécessaire dans les cas réfractaires ou chez les patients présentant des effets indésirables induits par les corticostéroïdes. L’objectif principal est d’éliminer toutes les cellules, minimisant ainsi les complications, y compris les cataractes, l’œdème maculaire cystoïde, l’hypotonie, la formation de synéchies ou le glaucome.,
Les Cycloplégiques aident à soulager la photophobie, secondaire au spasme ciliaire, et à prévenir et briser la formation de synéchies. Dans la plupart des cas, les gouttes à action courte, telles que le chlorhydrate de cyclopentolate à 1% ou le tropicamide à 1%, sont suffisantes. Ceux-ci permettent la motilité pupillaire et une récupération rapide lorsqu’ils sont arrêtés. Des cycloplégiques à action plus longue, tels que 5% d’homatropine, 0,25% de scopolamine et 1% d’atropine peuvent également être utiles. Si l’uvéite est plus sévère, une administration plus fréquente de cycloplégiques peut être nécessaire.,
Les corticostéroïdes topiques sont le pilier du traitement de l’uvéite, mais ils doivent être utilisés avec prudence en raison de leurs effets indésirables. L’objectif est d’utiliser la quantité minimale nécessaire pour contrôler l’inflammation et prévenir les complications. Un traitement initial agressif peut accélérer la récupération et limiter la durée du traitement. L’acétate de Prednisolone 1% donné toutes les heures est fortement recommandé pour les présentations aiguës. Habituellement, 2-3 semaines à la fréquence maximale est tout ce qui est nécessaire pour éliminer complètement toutes les cellules. Arrêtez toujours les corticostéroïdes en réduisant la dose.,
Les corticostéroïdes peuvent être administrés par 4 voies, y compris topique, périoculaire, intraoculaire (intravitréenne) et systémique. La thérapie topique est utilisée dans l’uvéite antérieure. Le dosage varie de toutes les heures à une fois par jour. La forme de pommade est disponible pour ceux qui ne peuvent pas tolérer le conservateur dans les gouttes et peut être particulièrement utile pour un dosage de coucher à action plus longue. Parfois, une inflammation sévère peut ne pas répondre et peut nécessiter des corticostéroïdes périoculaires, intraoculaires ou systémiques, en particulier si le segment postérieur est impliqué., Les corticostéroïdes périoculaires sont généralement administrés sous forme d’injections de dépôt dans l’espace sous-Tenon.
Les corticostéroïdes Intravitréens par injection ou par implantation d’un dispositif à libération prolongée se sont révélés utiles dans le traitement de l’uvéite chronique et de l’œdème maculaire cystoïde uvéitique. Ces dispositifs soutenus sont particulièrement prometteurs dans le traitement de l’inflammation de longue date, car ils peuvent libérer des médicaments aussi longtemps que plusieurs années après l’implantation., Cela permettrait de réduire ou d’éliminer les corticostéroïdes systémiques ou les agents immunosuppresseurs, minimisant ainsi les effets indésirables liés au traitement par ces agents. Comme pour tout traitement par corticostéroïdes, les pressions intraoculaires doivent être surveillées régulièrement.
Les corticostéroïdes systémiques peuvent être administrés par voie orale ou intraveineuse. Ceux-ci sont particulièrement bénéfiques lorsque la maladie systémique nécessite également une thérapie. Il est important de discuter des effets indésirables des corticostéroïdes avec le patient et de les faire surveiller par le médecin traitant du patient., La Prednisone à 1 mg / kg / J est une dose initiale utile.
une immunosuppression plus puissante peut être nécessaire chez les patients présentant une inflammation menaçant la vision qui interfère avec les activités de la vie quotidienne, un manque de réponse au traitement aux corticostéroïdes et une intolérance aux corticostéroïdes. Les Patients prenant 10 mg ou plus pour contrôler leurs symptômes peuvent bénéficier d’un antimétabolite en tant que traitement à long terme plus sûr. Les médicaments utilisés dans ces situations comprennent l’azathioprine, le mycophénolate mofétil, le cyclophosphamide, le chlorambucil, le méthotrexate, le tacrolimus et la cyclosporine., Ces agents sont généralement utilisés dans l’uvéite postérieure ou la panuvéite, mais ils peuvent parfois être nécessaires dans l’uvéite antérieure fibrineuse sévère associée à l’arthrite réactive ou à la spondylarthrite ankylosante.
la Cyclosporine devient de plus en plus utile comme adjuvant aux corticostéroïdes systémiques. Il peut permettre au médecin de diminuer ou de retirer totalement les corticostéroïdes une fois la rémission atteinte. La dose habituelle est de 2,5 à 5 mg/kg/J. une surveillance attentive de la pression artérielle et de la fonction rénale est requise. , Les thérapies expérimentales comprennent un dispositif à libération prolongée contenant de la cyclosporine ou le stéroïde hautement liposoluble fluocinolone et des anticorps monoclonaux contre la molécule CD4.
les thérapies Actuelles pour l’uvéite restent non spécifique dans leur mode d’action, et ils ont un certain nombre d’effets indésirables, comme déjà mentionné. Pour cette raison, plusieurs thérapies traitant de l’immunomodulation ont été étudiées. Deux traitements prometteurs impliquent le facteur de nécrose antitumorale alpha (anti-TNF-alpha) et l’utilisation d’un traitement de tolérance orale HLA-B27., Le TNF-alpha s’est avéré être un instigateur inflammatoire critique dans la pathogenèse de diverses formes d’uvéite, y compris L’AUA, dans des études animales et des études expérimentales humaines. Compte tenu de cela, des enquêtes ont été menées pour examiner l’efficacité et la sécurité de l’utilisation d’anti-TNF-alpha dans le traitement de diverses formes d’uvéite avec des résultats favorables. L’Infliximab est un anticorps monoclonal chimérique murin-humain dirigé contre le TNF-alpha humain., Il s’est avéré être un traitement rapide, efficace et sûr de l’inflammation oculaire menaçant la vision dans la maladie de Behcet et l’uvéite postérieure réfractaire.
L’étanercept est une protéine de fusion génétiquement modifiée, qui se lie et inactive à la fois le TNF-alpha et le TNF-bêta., Une étude a montré l’efficacité de cette protéine pour améliorer à la fois l’inflammation oculaire et l’inflammation articulaire lorsqu’elle est injectée par voie sous-cutanée deux fois par semaine pendant au moins 3 mois dans le traitement de l’uvéite chronique résistante, y compris l’uvéite antérieure chronique chez les enfants atteints d’uvéite rhumatoïde juvénile et d’uvéite idiopathique. Cela a permis la réduction des corticostéroïdes systémiques et / ou du méthotrexate systémique.
la tolérance orale consiste à administrer un antigène par voie orale pour induire une tolérance immunitaire périphérique spécifique., Les mécanismes de tolérance orale ne sont pas clairs, mais on pense qu’il implique un antigène spécifique et la génération d’une suppression active ou d’une anergie clonale dépendante de la dose d’antigène. La tolérance orale s’est avérée efficace dans des modèles expérimentaux traitant de la sclérose en plaques, de l’arthrite, du diabète, de la myasthénie grave et de l’uvéite., Sur cette base, des études cliniques ont été lancées en utilisant des antigènes tels que la myéline dans la sclérose en plaques, le collagène dans la polyarthrite rhumatoïde et les peptides uvéitogènes dans l’uvéite intermédiaire et postérieure, encore une fois avec succès et peu d’effets indésirables du traitement. Un peptide dérivé de HLA-B27 (B27PD) imitant l’autoantigène rétinien s’est avéré efficace chez les modèles animaux et les patients atteints d’uvéite.
D’autres options thérapeutiques émergentes incluent l’antibiothérapie compte tenu du rôle impliqué des infections bactériennes à gram négatif sur le déclenchement de L’AUA associée à HLA-B27., Le traitement par la Sulfasalazine a été étudié pour son rôle potentiel dans la réduction du nombre d’attaques récurrentes d’AUA, et la ciprofloxacine prophylactique a également été étudiée mais n’a pas été jugée bénéfique compte tenu de ses effets indésirables et de son coût.
Les futurs nouveaux traitements potentiels reposeront sur une meilleure compréhension du système immunitaire et incluront des substances telles que les cytokines, les chimiokines, les molécules d’adhésion cellulaire et les sous-ensembles de lymphocytes T.,
le rôle du rhumatologue dans la prise en charge de l’AUA est important pour identifier les maladies systémiques sous-jacentes qui peuvent être présentes et pour surveiller le traitement immunosuppresseur ultérieur.