Comme on peut s’y attendre, les superacides sont des acides extrêmement forts, Beaucoup plus forts que les acides minéraux forts traditionnels tels que l’acide sulfurique et l’acide chlorhydrique.
L’acidité fait référence à la capacité d’ajouter des protons, H+, à d’autres substances: plus l’acide est fort, plus son pouvoir de protoner d’autres substances est important.
un superacide est défini comme une substance qui a un potentiel chimique H+ plus élevé que l’acide sulfurique pur à 100%.,

List of Superacids
| Substance | Formula | H0 | |
|---|---|---|---|
| Chlorosulfuric acid | HSO3Cl 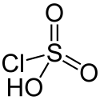 |
-12.8 | Reacts with alcohols to produce alkyl sulfate detergents. |
| Triflic acid | CF3SO3H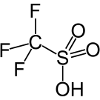 |
-14.1 | Also known as trifluoromethanesulfonic acid, or TFMS., Réagit avec les alcools pour produire des éthers et des oléfines. |
| Oleum | H2SO4 + SO3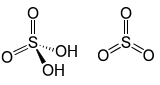 |
-15 | le trioxyde de soufre dissous dans l’acide sulfurique pur produit de l’oléum, qui est une méthode préférée, par dilution avec de l’eau, pour produire de l’acide sulfurique concentré.L’oléum est également utilisé comme réactif dans la fabrication d’explosifs tels que la nitrocellulose. |
| Fluorosulfuric acide | HSO3F 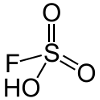 |
-15.,1 | est utilisé pour préparer l’acide magique (voir ci-dessous) et pour régénérer les mélanges HF et H2SO4 utilisés pour graver le verre au plomb. |
| acide Carborane | H(CHB11X11) |
-18.0 | le carborane montré à gauche est fluoré; les carboranes chlorés sont également des superacides, mais avec une acidité plus faible.L’acide carborane fluoré est le seul acide capable de protonater le CO2 pour produire +.Le Carborane est le seul acide capable de protoner le C60 sans réactions secondaires.Le Carborane protonate le benzène pour donner du sel C6H7+.,Bien qu’ils aient un grand pouvoir protonant, les carboranes sont moins corrosifs que les autres superacides; contrairement à la plupart, ils peuvent être stockés dans une bouteille en verre. |
| acide magique | FSO3H·SbF5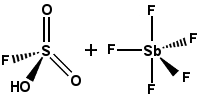 |
-19.2 | préparé à partir d’acide fluorosulfurique (voir ci-dessus) et de pentafluorure d’antimoine. Catalyse l’isomérisation des hydrocarbures saturés, stabilise les carbocations. |
| acide Fluoroantimonique | h2fsbf6 ou H2F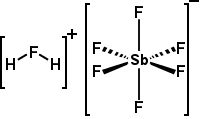 |
-31.,3 | superacide le plus puissant, il est produit en faisant réagir un rapport mole 2:1 de HF avec SbF5. Peut protoner presque n’importe quel composé organique. |
l’Acidité est indiqué par l’acidité de Hammett fonction, H0.
comme le pH, H0 est une mesure de l’acidité; des valeurs plus faibles de H0 signifient un pouvoir protonant plus élevé.Comme pH, H0 est une échelle logarithmique.
100% d’acide sulfurique a un H0 de -12.Comparez cela avec l’acide fluoroantimonique H0 de -31.Cela signifie que l’acide fluoroantimonique est 1019 plus acide que l’acide sulfurique pur., C’est une grande différence qu’il existe entre la taille du soleil et de la taille d’une amibe.
