qu’est-ce qu’un Ion?
Un ion est un atome ou une molécule qui porte une charge électrique.
les Ions sont identifiés par l’utilisation d’un symbole pour montrer le signe et la taille de leur charge électrique.
Anions et Cations
Les ions chargés négativement sont appelés anions, et les ions chargés positivement sont appelés cations.,l’atome n gagne trois électrons pour devenir N3-
exemples de Cations
- Un atome de sodium perd un électron pour devenir Na+
- Un atome de magnésium perd deux électrons pour>un atome de fer perd trois électrons pour devenir Fe3+
- l’eau réagit avec H+pour former le cation moléculaire H3O+
formation d’ions
la formation d’ions minimise ainsi l’énergie potentielle totale des espèces chimiques impliquées dans la réaction chimique.,Souvent, cela est réalisé en permettant aux atomes de différents éléments d’obtenir une enveloppe complète d’électrons.
considérons le fluorure de lithium de sel:
Les atomes de Lithium ont 3 électrons, ce qui signifie qu’ils ont des électrons dans deux coquilles: 2 dans la première coquille et 1 dans la second.By perdant un électron pour devenir un cation, le lithium obtient un arrangement d’électrons stable, identique à celui de l’hélium de gaz noble.,
Li Atom
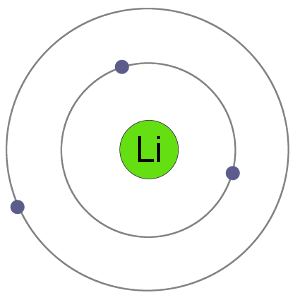
Li+ Cation
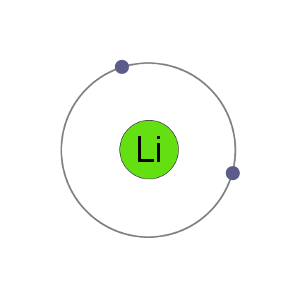
des atomes de Fluor ont 9 électrons, ce qui signifie qu’ils ont 2 dans la première enveloppe et 7 dans le second.By gagner un électron pour devenir un anion de l’ion fluorure obtient un stable de l’électron arrangement, identique à celui de la noblesse, du gaz néon., »e9c2d99c83″>
et ainsi la réaction redox du sodium avec le chlore pour former un composé ionique est énergétiquement favorable:
réduction du chlore: CL2 + 2e- → 2cl-
réaction globale: 2na + CL2 → 2NaCl
tailles d’ions
les cations sont plus petits que atome – considérez comment l’atome de sodium a des électrons dans trois coquilles, tandis que l’ion de sodium a des électrons dans seulement deux coquilles.,Avec plus d’électrons, les anions sont plus grands que l’atome d’origine.
Les tailles D’ions sont mesurées par le rayon ionique.
rayons ioniques dans les Picomètres
La couleur grise dans les diagrammes montre la taille de l’atome d’origine. Le bleu (cation) et le jaune (anion) indiquent la taille de l’ion. (Diagrammes de Chris King.)

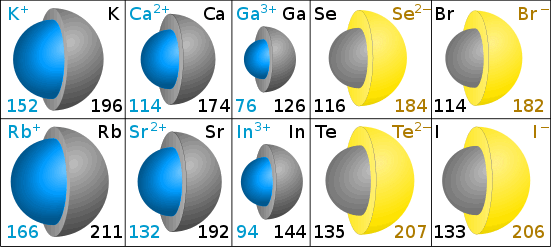
Composés Ioniques
composés Ioniques, tels que le chlorure de sodium (NaCl) sont formées en raison de l’attraction électrostatique entre les anions et les cations.,Les composés ioniques sont électriquement neutres, car le nombre total de charges positives et le nombre total de charges négatives sont toujours égaux.
compte tenu des éléments chimiques, la tendance la plus élevée à former des composés ioniques existe dans les métaux les moins électronégatifs et les non-métaux les plus électronégatifs.
conducteurs électriques
Les Ions peuvent transporter du courant électrique; cela peut être observé dans les cellules électrochimiques, et dans le plasma, par exemple.
en général, les composés ioniques solides ne transportent pas de courant électrique, car les ions sont bloqués dans des positions fixes dans un réseau cristallin.,Les composés ioniques ne conduisent l’électricité qu’en fusion ou en solution, lorsque les ions sont libérés du réseau cristallin et deviennent mobiles.