La Chaleur et la température sont un sujet étroitement lié, et en tant que tel, la différence entre les deux peut être un peu déroutante. La principale différence est que la chaleur traite de l’énergie thermique, alors que la température est plus concernée par l’énergie cinétique moléculaire.
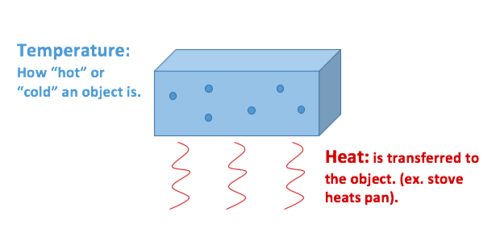
Chaleur est un transfert d’énergie thermique, alors que la température est une propriété de l’objet d’expositions.
quel est la différence?,
La Chaleur décrit le transfert d’énergie thermique entre molécules dans un système et est mesurée en Joules. La chaleur mesure la façon dont l’énergie se déplace ou circule. Un objet peut gagner de la chaleur ou perdre de la chaleur, mais il ne peut pas avoir de chaleur. La chaleur est une mesure du changement, jamais une propriété possédée par un objet ou un système. Par conséquent, il est classé comme une variable de processus.
la température décrit l’énergie cinétique moyenne des molécules dans un matériau ou un système et est mesurée en Celsius (°C), Kelvin(K), Fahrenheit (°F) ou Rankine (R)., C’est une propriété physique mesurable d’un objet—également connue sous le nom de variable d’état. D’autres propriétés physiques mesurables incluent la vitesse, la masse et la densité, pour n’en nommer que quelques-unes.
similitudes
La Chaleur est un transfert d’énergie thermique causé par une différence de température entre les molécules.
Remarque:
l’énergie thermique peut être autrement comprise comme l’énergie cinétique et potentielle microscopique totale d’un système.,
Deuxième Loi de la Thermodynamique
La seconde loi de la thermodynamique est un sujet complexe qui nécessite une étude intensive dans le domaine de la thermodynamique pour vraiment comprendre. Cependant, aux fins de cet article, un seul petit aspect doit être compris et c’est le fait que la chaleur coulera toujours spontanément des substances plus chaudes vers des substances plus froides. Cette déclaration simple explique pourquoi un glaçon ne se forme pas à l’extérieur par une journée chaude ou pourquoi il fond lorsqu’il est déposé dans un bol d’eau tiède.,
expérience de pensée
imaginez le glaçon susmentionné tombé dans un bol d’eau chaude—la glace doit gagner de la chaleur (énergie thermique) de l’eau dans le bol (voir paragraphe précédent). L’ajout d’énergie thermique entraîne une augmentation de l’énergie cinétique de la molécule de glace, et donc une augmentation de la température. Ceci est connu car la température est en fait la mesure de l’énergie cinétique moyenne des molécules. De plus, la glace continuera à gagner de l’énergie thermique, ce qui fera que ses molécules se déplaceront plus rapidement et finiront par briser leurs liaisons intermoléculaires ou fondre.,
En conclusion, le transfert de chaleur ou d’énergie thermique modifiera généralement la température de la substance, mais pas toujours! Par exemple, au moment où la glace dans le bol se transforme en eau, Ces molécules d’eau seront exactement à la même température que lorsqu’elles étaient de la glace. Dans ce cas, au lieu que l’énergie thermique fasse un travail pour augmenter l’énergie cinétique, elle fonctionne pour briser les liaisons intermoléculaires, provoquant un changement d’état., Cependant, au fil du temps, la température de la glace récemment fondue augmentera jusqu’à ce que tout dans le bol atteigne l’équilibre—ce qui signifie une température constante tout au long.
Pour en savoir Plus
- la Chaleur
- Température
- l’énergie Thermique
- l’énergie Cinétique
- Intérieur de l’énergie
- Ou explorer une page au hasard