Pyridinium chlorochromate (PCC) is a milder version of chromic acid.
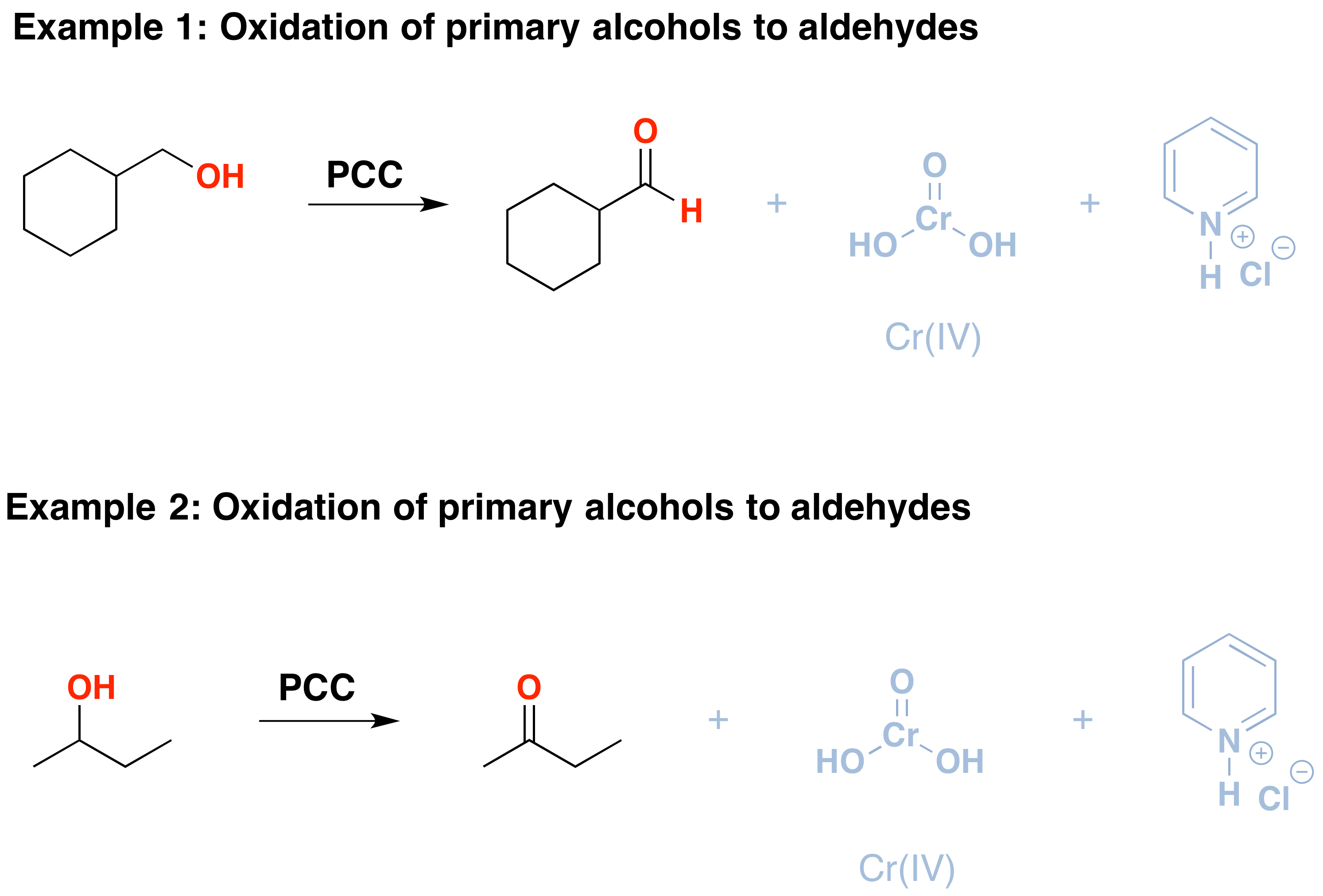
PCC oxidizes alcohols one rung up the oxidation ladder, from primary alcohols to aldehydes and from secondary alcohols to ketones. In contrast to chromic acid, PCC will not oxidize aldehydes to carboxylic acids., Similar o igual a: \(CrO_3\) y piridina (el reactivo de Collins) también oxidará alcoholes primarios a aldehídos. Aquí hay dos ejemplos de PCC en acción.
- si agrega un equivalente de PCC a cualquiera de estos alcoholes, se producirá la versión oxidada. Los subproductos (presentados en gris) son Cr(IV), así como el clorhidrato de piridinio.
- hay que tener cuidado con la cantidad de agua presente en la reacción., Si el agua está presente, puede agregarse al aldehído para crear el hidrato, que podría oxidarse aún más por un segundo equivalente de PCC si está presente. Esto no es una preocupación con cetonas debido a que no hay H pegado directamente a C.
¿Cómo funciona? Las reacciones de oxidación de este tipo son en realidad un tipo de reacción de eliminación. La reacción comienza con un enlace simple carbono-oxígeno y resulta en un enlace doble carbono-oxígeno., La reacción de eliminación puede ocurrir debido al buen grupo de salida en el oxígeno, es decir, el cromo, que se desplazará cuando el enlace C-H vecino se rompe con una base.
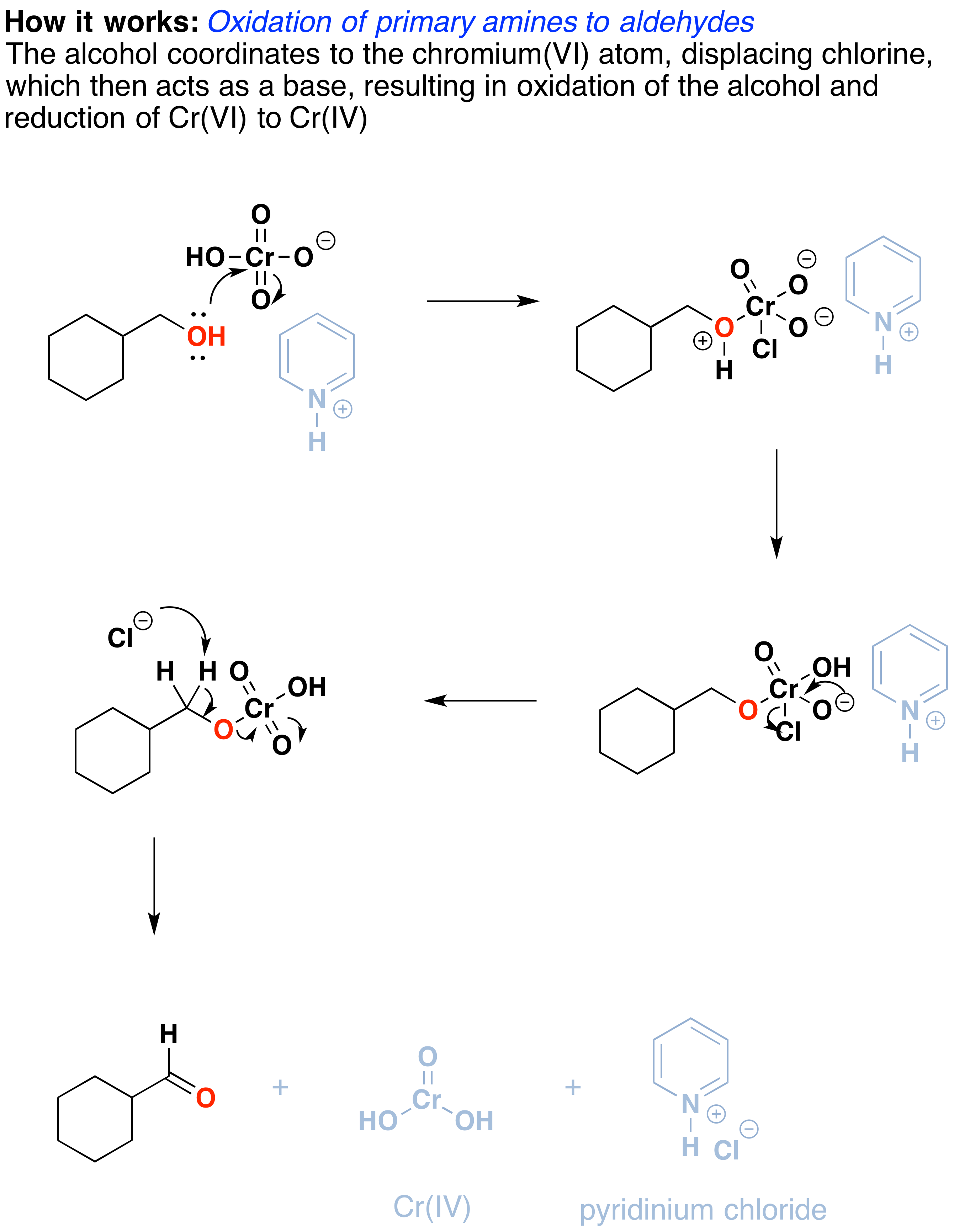
El primer paso es el ataque del oxígeno sobre el cromo para formar el Cr-O bonos. En segundo lugar, un protón en el (ahora positivo) OH se transfiere a uno de los oxígenos del cromo, posiblemente a través de la intermediación de la sal de piridinio., Un ion cloruro es entonces desplazado en una reacción que recuerda a una reacción de eliminación de 1,2 para formar lo que se conoce como éster de cromato.
el doble enlace C-O se forma cuando una base elimina el protón en el carbono adyacente al oxígeno. Los electrones del enlace C-H se mueven para formar el enlace C-O, y en el proceso, el enlace o-Cr se rompe, y Cr (VI) se convierte en Cr(IV) (dibujado aquí como o=Cr(OH) 2).,
notas de la vida Real: si terminas usando PCC en el laboratorio, no olvides agregar tamices moleculares o Celite o algún otro sólido al fondo del matraz porque de lo contrario obtendrás un desagradable alquitrán marrón que es difícil de limpiar. La toxicidad y el desorden asociados con el cromo ha estimulado el desarrollo de otras alternativas, como TPAP, IBX, DMP y una gran cantidad de otros reactivos que generalmente no se aprenden hasta la escuela de posgrado.
Colaboradores
-
James Ashenhurst (MasterOrganicChemistry.com)