Schritt 1
Im ersten Schritt entnimmt die Ethansäure ein Proton (ein Wasserstoffion) aus der konzentrierten Schwefelsäure. Das Proton wird an eines der einsamen Paare des Sauerstoffs gebunden, der doppelt mit dem Kohlenstoff verbunden ist.
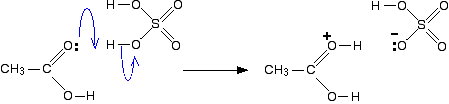
Die Übertragung des Protons auf den Sauerstoff gibt ihm eine positive Ladung, aber es ist tatsächlich irreführend, die Struktur auf diese Weise zu zeichnen (obwohl fast jeder tut!).,
Die positive Ladung wird über das gesamte rechte Ende des Ions delokalisiert, mit einer angemessenen Menge an Positivität auf dem Kohlenstoffatom. Mit anderen Worten, Sie können sich eine Elektronenpaarverschiebung vorstellen, um diese Struktur zu erhalten:
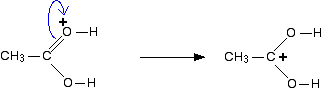
Sie könnten sich auch eine andere Elektronenpaarverschiebung vorstellen, die eine dritte Struktur erzeugt:
Welche davon ist die richtige Struktur des gebildeten Ions? Keiner von ihnen! Die Wahrheit liegt irgendwo zwischen ihnen allen., Eine Möglichkeit, die delokalisierte Struktur des Ions zu schreiben, ist wie folgt:
Die doppelköpfigen Pfeile sagen Ihnen, dass jede der einzelnen Strukturen einen Beitrag zur realen Struktur des Ions leistet. Sie bedeuten nicht, dass die Bindungen zwischen einer Struktur und einer anderen hin und her kippen. Die verschiedenen Strukturen sind als Resonanzstrukturen oder kanonische Formen bekannt.
Es wird sowohl auf den Sauerstoffatomen als auch auf dem Kohlenstoffatom eine gewisse positive Ladung vorhanden sein., Jede der Bindungen zwischen dem Kohlenstoff und den beiden Oxygenen ist gleich – irgendwo zwischen einer einzigen Bindung und einer Doppelbindung.