Abbildung 4.1 (siehe vergrößerte Ansicht)
Deshalb ein Verständnis der synapse führt zu einem Verständnis der anderen. Daher werden wir zuerst den Prozess der synaptischen Übertragung am neuromuskulären Knotenpunkt des Skeletts diskutieren.,
Die Merkmale des synaptischen Übergangs am neuromuskulären Übergang sind in der Abbildung links dargestellt. Skelettmuskelfasern werden von Motoneuronen innerviert, deren Zellkörper sich im ventralen Horn des Rückenmarks befinden. Die terminale Region des Axons führt zu sehr feinen Prozessen, die entlang der Skelettmuskelzellen verlaufen. Entlang dieser Prozesse befinden sich spezialisierte Strukturen, die als Synapsen bezeichnet werden. Die besondere Synapse, die zwischen einem spinalen Motoneuron und einer Skelettmuskelzelle hergestellt wird, wird aufgrund ihrer spezifischen Struktur als motorische Endplatte bezeichnet.,
Die Synapse am neuromuskulären Übergang weist drei charakteristische Merkmale chemischer Synapsen im Nervensystem auf. Erstens gibt es eine deutliche Trennung zwischen der präsynaptischen und der postsynaptischen Membran. Der Raum zwischen den beiden ist als synaptischer Spalt bekannt. Der Raum sagt uns, dass es einen intermediären Signalmechanismus zwischen dem präsynaptischen Neuron und dem postsynaptischen Neuron geben muss, um Informationsfluss über den synaptischen Spalt zu haben. Zweitens gibt es eine charakteristische hohe Dichte kleiner kugelförmiger Vesikel., Diese synaptischen Vesikel enthalten Neurotransmittersubstanzen. Synapsen sind auch mit einer hohen Dichte von Mitochondrien verbunden. Drittens kommt es in den meisten Fällen zu einer charakteristischen Verdickung der postsynaptischen Membran, was zumindest teilweise darauf zurückzuführen ist, dass die postsynaptische Membran eine hohe Dichte spezialisierter Rezeptoren aufweist, die die aus dem präsynaptischen Neuron freigesetzten chemischen Sendersubstanzen binden. Weitere Details zu den morphologischen Merkmalen synaptischer Verbindungen finden Sie in Kapitel 8 und Kapitel 10.
4.,2 Physiologie der synaptischen Transmission am neuromuskulären Übergang
Abbildung 4.2
Die Abbildung rechts veranschaulicht sehr schematisch, wie es möglich ist, die Physiologie der synaptischen Transmission am neuromuskulären Skelett-Übergang im Detail zu untersuchen. Ein Stück Muskel und sein angebrachter Nerv werden in eine kleine Versuchskammer gelegt, die mit einer geeigneten Klingellösung gefüllt ist. Das Ruhepotential der Muskelzelle wird mit einer Mikroelektrode aufgezeichnet. Elektroden werden auch auf der Oberfläche des Nervenaxons platziert., Kurze Elektroschocks führen dazu, dass Aktionspotentiale initiiert werden, die sich zum synaptischen Terminal ausbreiten.
Die folgende Abbildung veranschaulicht zwei Arten potenzieller Veränderungen, die in einer solchen isolierten Nerven-Muskel-Vorbereitung aufgezeichnet wurden. Das Experiment zeigt auch die Eigenschaften eines starken Medikaments, Curare, das sich als sehr nützlich erwiesen hat, um den Prozess der synaptischen Übertragung am neuromuskulären Knotenpunkt des Skeletts zu untersuchen. Teil A veranschaulicht die Abfolge potenzieller Veränderungen, die in der Muskelzelle als Folge der Stimulierung des motorischen Axons aufgezeichnet wurden., Der Pfeil zeigt den Zeitpunkt an, zu dem der Schock an das Motoraxon abgegeben wird. Beachten Sie, dass es nach dem Schock eine Ruhephase gibt. Die Verzögerung ist auf die Zeit zurückzuführen, die es dauert, bis sich das Aktionspotential im Motoraxon von seinem Initiationsort ausbreitet. Nach der Verzögerung werden zwei Arten von Potentialen in der Muskelzelle aufgezeichnet. Erstens gibt es ein sich relativ langsam veränderndes Potenzial, das im Mittelpunkt der folgenden Diskussion stehen wird., Wenn dieses langsame Anfangspotential ausreichend groß ist, wie es normalerweise in Skelettmuskelzellen der Fall ist, wird ein zweites Potential, ein Aktionspotential, in der Muskelzelle ausgelöst.
Abbildung 4.3
Aktionspotentiale in Skelettmuskelzellen beruhen auf ionischen Mechanismen, die denen ähneln, die zuvor diskutiert wurden. Insbesondere gibt es eine spannungsabhängige Änderung der Na+-Permeabilität, gefolgt von einer verzögerten Erhöhung der K+ – Permeabilität. (Bei glatten Muskelzellen und Herzmuskelzellen sind die Ionenmechanismen jedoch unterschiedlich.,)
Das zugrunde liegende Ereignis, das das Aktionspotential auslöst, kann durch die Nutzung von Curare, einem Pfeilgift, das von einigen südamerikanischen Indianern verwendet wird, aufgedeckt werden. Eine niedrige Dosis von Curare (Teil B) reduziert das zugrunde liegende Ereignis, ist jedoch immer noch nicht ausreichend reduziert, um den Schwellenwert zu unterschreiten. Wenn eine etwas höhere Dosis Curare abgegeben wird (Teil C), wird das langsame zugrunde liegende Ereignis unterschwellig. Das zugrunde liegende Signal wird als Endplattenpotential (EPP) bezeichnet, da es sich um eine Potentialänderung handelt, die an der Motorendplatte aufgezeichnet wird. Im Allgemeinen ist es als exzitatorisches postsynaptisches Potential (EPSP) bekannt.,
Curare blockiert das Endplattenpotential, da es ein kompetitiver Inhibitor von Acetylcholin (ACh) ist, dem Transmitter, der am präsynaptischen Terminal freigesetzt wird. Curare blockiert nicht die spannungsabhängige Na+ Leitfähigkeit oder die spannungsabhängige K+ Leitfähigkeit, die dem Muskelaktionspotential zugrunde liegt. Curare beeinflusst den Reiz (die EPSP), der normalerweise zur Einleitung des Muskelaktionspotentials führt. Ein mit Curare vergiftetes Tier erstickt, weil der Prozess der neuromuskulären Übertragung an den Atemmuskeln blockiert ist.,
Normalerweise ist die Größe des Endplattenpotentials ziemlich groß. Tatsächlich beträgt die Amplitude des Endplattenpotentials etwa 50 mV, aber nur etwa 30 mV werden benötigt, um die Schwelle zu erreichen. Die zusätzlichen 20 mV werden als Sicherheitsfaktor bezeichnet. Selbst wenn das Endplattenpotential aufgrund von Ermüdung etwas kleiner werden würde (z. B. 40 mV Amplitude), würde die EPP daher die Schwelle erreichen und die Eins-zu-Eins-Beziehung zwischen einem Aktionspotential im Motoraxon und einem Aktionspotential in der Muskelzelle würde erhalten bleiben.
Abbildung 4.4
4.,3 Ausbreitung der EPP
Was sind die Eigenschaften der EPP und wie vergleicht sie sich mit den Eigenschaften des Aktionspotentials?
Ist das Endplattenpotential auf eine spannungsabhängige Änderung der Na+-und K+ – Permeabilitäten wie das Aktionspotential zurückzuführen?
Wird das Endplattenpotential in einer Alles-oder-Nichts-Weise wie das Aktionspotential propagiert?
Die Abbildung links zeigt ein Experiment, das die Ausbreitung des Endplattenpotentials untersucht. Die Muskelfaser wird wiederholt mit Elektroden im Abstand von 1 mm aufgespießt., (Beachten Sie, dass das Endplattenpotential klein ist, da dieses Experiment in Gegenwart einer niedrigen Konzentration von Curare durchgeführt wird, so dass das Endplattenpotential ohne die Komplikationen der Auslösung eines Aktionspotentials aufgezeichnet werden kann.) Das Endplattenpotential wird nicht ganz oder gar nicht propagiert. Es breitet sich entlang des Muskels aus, aber es tut dies mit Dekrement., Somit erfolgt die Ausbreitung des Endplattenpotentials von seiner Initiationsstelle auf andere Stellen entlang der Muskelzelle passiv und mit Dekrement, ebenso wie sich eine unterschwellige Potentialänderung in einem Teil des Axons entlang des Axons ausbreitet, oder ebenso wie sich eine Temperaturänderung an einem Punkt auf einem Metallstab entlang des Stabes ausbreitet.
4.4 Überblick über die Abfolge der dem EPP zugrunde liegenden Ereignisse
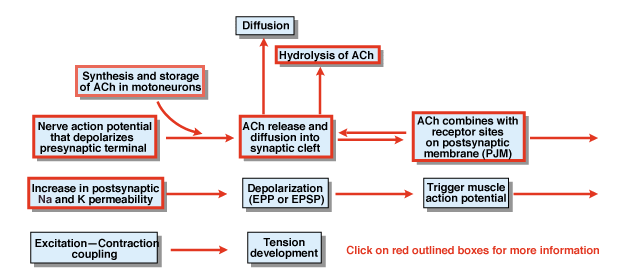
Abbildung 4.5
Was sind die anderen Schritte im Prozess der chemischen synaptischen Übertragung? Abbildung 4.,5 bietet einen Überblick. Ein Nervenaktionspotential, das im Zellkörper eines spinalen Motoneurons ausgelöst wird, breitet sich aus den ventralen Wurzeln aus und dringt schließlich in die synaptischen Terminals der Motoneuronen ein. Infolge des Aktionspotentials wird der chemische Transmitter Acetylcholin (ACh) in den synaptischen Spalt freigesetzt. ACh diffundiert über den synaptischen Spalt und bindet an spezielle Rezeptoren auf der postsynaptischen oder der postjunktionellen Membran. Die Bindung von ACh an seine Rezeptoren bewirkt eine Konformationsänderung in einem Membrankanal, der spezifisch sowohl für Na+ als auch für K+durchlässig ist., Infolge einer Erhöhung der Na+ – und K+ – Permeabilität kommt es zu einer Depolarisation der postsynaptischen Membran. Diese Depolarisation wird als Endplattenpotential oder allgemeiner als EPSP bezeichnet. Wenn der EPSP ausreichend groß ist, wie er sich normalerweise am neuromuskulären Übergang befindet, führt dies zur Einleitung eines Aktionspotentials in der Muskelzelle. Das Aktionspotential initiiert den Prozess der Erregungskontraktionskopplung und die Entwicklung von Spannung. Die Dauer des Endplattenpotentials beträgt etwa 10 msec.
Zwei Faktoren steuern die Dauer des EPSP am neuromuskulären Übergang., Zuerst wird ACh durch Diffusion entfernt. Zweitens hydrolysiert oder bricht eine Substanz im synaptischen Spalt, Acetylcholinesterase (AChE) genannt, ACh. Schmerz ist eines der effizientesten bekannten Enzyme. Ein einzelnes Schmerzmolekül kann 600.000 Moleküle ACh pro Minute hydrolysieren.
4.5 Rolle des Schmerzes
Abbildung 4.6
Eine wichtige Familie von Substanzen, von denen einer Neostigmin ist, hemmt die Wirkung von Schmerzen. Neostigmin blockiert die Wirkung von Schmerzen und macht dadurch das Endplattenpotential größer und länger., Diese Abbildung zeigt zwei Endplattenpotentiale. Eine wurde in Kochsalzlösung und Curare aufgenommen und eine zweite nach Zugabe von Neostigmin zu der Lösung. (Curare wird hinzugefügt, damit die Eigenschaften des EPP untersucht werden können, ohne ein Aktionspotential in der Muskelzelle auszulösen.) Nach der Anwendung von Neostigmin ist das Endplattenpotential viel größer und länger.
4.6 a Myasthenia Gravis
Myasthenia gravis ist aufgrund einer Abnahme der Anzahl von Acetylcholinrezeptoren in der Muskelzelle mit schwerer Muskelschwäche verbunden., Wenn das Endplattenpotential kleiner ist, erreicht das Endplattenpotential den Schwellenwert nicht. Wenn es die Schwelle nicht erreicht, gibt es kein Aktionspotential in der Muskelzelle und keine Kontraktion des Muskels, was zu Muskelschwäche führt. Neostigmin und andere Schmerzhemmer werden zur Behandlung von Patienten mit Myasthenia gravis eingesetzt. Diese Mittel lassen die Menge an Acetylcholin, die effektiver freigesetzt wird, die verbleibenden Acetylcholinrezeptoren erreichen.
4.,6b Nervenmittel
Obwohl Inhibitoren von Schmerzen einen wichtigen therapeutischen Wert haben, wurden und werden einige Inhibitoren immer noch als Gifte verwendet. Einige Schmerzhemmer wie Soman und Sarin bilden einen ziemlich irreversiblen Schmerzblock. Dieser Block führt zu extremen ACh-Spiegeln im synaptischen Spalt. Personen, die so vergiftet sind, sterben an Anfällen und Muskelspastizität, einschließlich der Atemmuskulatur.
Abbildung 4.7
4.,7 Iontophorese von ACh
Die Iontophorese ist eine interessante Technik, mit der die Hypothese, dass ACh die Neurotransmittersubstanz am neuromuskulären Übergang ist, weiter getestet werden kann. Wenn ACh der Sender ist, der von dieser Synapse freigesetzt wird, würde man vorhersagen, dass es möglich sein sollte, künstliche Anwendung des Senders für die normale Freisetzung des Senders zu ersetzen. Da ACh ein positiv geladenes Molekül ist, kann es aus einer Mikroelektrode herausgedrückt werden, um die Freisetzung von ACh aus einem präsynaptischen Terminal zu simulieren.
Abbildung 4.,8
Tatsächlich können winzige Mengen ACh in der Nähe des neuromuskulären Übergangs angewendet werden. Abbildung 4.8 vergleicht eine EPP, die durch Stimulation des motorischen Axons und die Reaktion auf ACh-Auswurfe erzeugt wird. Die Potentialänderung sieht fast identisch aus mit dem Endplattenpotential, das durch die normale Freisetzung von ACh erzeugt wird. Dieses Experiment bietet experimentelle Unterstützung für das Konzept, dass ACh der natürliche Sender an dieser Synapse ist.,
Die Reaktion auf den Auswurf von ACh hat einige andere interessante Eigenschaften, die alle mit der cholinergen Natur der Synapse am neuromuskulären Skelettknotenpunkt übereinstimmen. Neostigmin macht die Reaktion auf die Iontophorese von ACh länger und größer. Curare reduziert die Reaktion, weil es mit der normalen Bindung von ACh konkurriert. Wenn ACh in die Muskelzelle ausgestoßen wird, passiert nichts, weil die Rezeptoren für Acetylcholin nicht im Inneren sind; sie sind auf der Außenseite der Muskelzelle., Die Anwendung von Acetylcholin auf Muskelregionen abseits der Endplatte führt zu keiner Reaktion, da die Rezeptoren für das ACh im synaptischen Bereich konzentriert sind.
Um Ihr bisheriges Verständnis zu testen, überlegen Sie, wie sich ein Wirkstoff wie TTX auf die Erzeugung eines EPP und die Reaktion einer Muskelfaser auf die iontophoretische Anwendung von ACh auswirken würde. TTX hat keinen Einfluss auf die Reaktion auf ACh, blockiert jedoch die EPP. Der Grund, warum die Reaktion auf ACh nicht betroffen ist, ist klar, aber viele erwarten, dass es auch keine Auswirkungen auf die EVP geben sollte, wenn hier keine Auswirkungen auftreten., Tetrodotoxin beeinflusst die Bindung von Acetylcholin an die Rezeptoren nicht und beeinflusst daher nicht die Reaktion auf die direkte Anwendung von ACh. Tetrodotoxin beeinflusst jedoch die Fähigkeit eines Aktionspotentials, im motorischen Axon ausgelöst zu werden. Wenn im Motoraxon kein Aktionspotential ausgelöst werden kann, kann dies nicht zur Freisetzung des Senders führen. Somit würde Tetrodotoxin die EPP vollständig abschaffen. Der Block wäre nicht auf einen Block von ACh-Rezeptoren zurückzuführen, sondern auf einen Block eines Schrittes vor der Freisetzung des Senders.
4.,8 Ionische Mechanismen der EPP
Bernard Katz und seine Kollegen waren Pioniere bei der Untersuchung von Mechanismen der synaptischen Übertragung am neuromuskulären Übergang. Sie schlugen vor, dass der von ACh geöffnete Kanal eine war, die sowohl Na+ als auch K+gleich durchlässig war. Da es für Na+ und K+ gleichermaßen durchlässig war, schlug Katz vor, dass sich das Membranpotential infolge der Öffnung dieser Kanäle in Richtung 0 mV bewegen würde. (Ein Wert von Alpha in der GHK-Gleichung gleich eins, der, wenn er in die Gleichung ersetzt wird, ein Potential von etwa 0 mV ergibt.,)
Abbildung 4.9
Das in der Abbildung links gezeigte Experiment testet dieses Konzept. Die Muskelzelle wurde mit einer Aufzeichnungselektrode sowie einer weiteren Elektrode durchdrungen, die mit einer geeigneten Potentialquelle verbunden werden kann, um das Membranpotential künstlich zu verändern. Normalerweise beträgt das Membranpotential wieder etwa -80 mV, eine kleine Menge Curare wird hinzugefügt, so dass die EPP klein ist. Katz bemerkte in diesen Experimenten, dass sich die Größe der EPP in Abhängigkeit vom Potenzial der Muskelzelle dramatisch veränderte., Wenn das Membranpotential auf 0 mV bewegt wird, wird keinerlei Potentialänderung aufgezeichnet. Wenn das Membranpotential +30 mV beträgt, wird der EPP invertiert. So erzeugen drei verschiedene Reize Endplattenpotentiale, die sich stark voneinander unterscheiden.
Das Fehlen einer Antwort, wenn das Potential bei 0 mV liegt, ist besonders aussagekräftig. Überlegen Sie, warum keine mögliche Änderung aufgezeichnet wird. Vermutlich wird der Sender freigesetzt und an die Rezeptoren gebunden., Die einfache Erklärung für einen Mangel an potenziellen Veränderungen ist, dass das Potenzial, mit dem die Öffnung der ACh-Kanäle zu erreichen versucht, bereits erreicht wurde. Wenn das Membranpotential positiver als 0 mV ist, wird die EPP invertiert. Unabhängig vom Potential neigt die Änderung der Permeabilität dazu, das Membranpotential in Richtung 0 mV zu bewegen! Wenn das Ruhepotential negativer als 0 mV ist, gibt es eine Ablenkung nach oben. Wenn es positiver ist, gibt es eine Abwärtsauslenkung. Wenn es bereits bei 0 mV ist, gibt es keine Durchbiegung.
Abbildung 4.,10
Dieses Potential wird auch als Umkehrpotential bezeichnet, da es das Potential ist, bei dem sich das Vorzeichen des synaptischen Potentials umkehrt. Das Experiment zeigt, dass bestimmte Kanäle infolge der ACh-Bindung an Rezeptoren für Na+ und K+gleichermaßen durchlässig werden. Diese Permeabilitätsänderung neigt dazu, das Membranpotential von dort, wo es anfänglich ist, in Richtung eines neuen Potentials von 0 mV zu bewegen.
Warum erreicht das normale Endplattenpotential eigentlich nie 0 mV?, Ein Grund dafür ist, dass die Reihenfolge der Permeabilitätsänderungen, die dem Aktionspotential zugrunde liegen, die von der EPP erzeugten Änderungen „überschwemmen“. Aber selbst wenn ein Aktionspotential nicht ausgelöst würde, würde die EVP immer noch nicht 0 mV erreichen. Dies liegt daran, dass die ACh-Kanäle nur ein kleiner Bruchteil der Gesamtzahl der Kanäle in Muskelfasern sind. Die K+ Kanäle, die eine Muskelzelle mit ihrem Ruhepotential ausstatten, sind ebenfalls vorhanden. Ihre Aufgabe ist es zu versuchen, die Zelle am Ruhepotential zu halten.,
Der von ACh geöffnete Kanal ist Mitglied einer allgemeinen Klasse von Kanälen, die als Liganden-gated Channels oder ionotrope Rezeptoren bezeichnet werden. Wie in Abbildung 4.10 dargestellt, ist die Senderbindungsstelle Teil des Kanals selbst. Infolge der Transmitter-Bindung an den Rezeptor (im Allgemeinen sind zwei Moleküle notwendig) gibt es eine Konformationsänderung im Protein, die es ermöglicht, dass sich ein Porenbereich öffnet und Ionen ihre elektrochemischen Gradienten herunterfließen. Weitere details des Kanals sind in Kapitel 11.,
Testen Sie Ihr Wissen
- Frage 1
- A
- B
- C
- D
Ein Endplat-Potential in einer Skelettmuskelzelle könnte prinzipiell durch eine verminderte Permeabilität für welche der folgenden Ionen erzeugt werden? (Nehmen wir an, dass es eine endliche anfängliche Permeabilität für jedes der unten aufgeführten Ionen gibt und dass physiologische Konzentrationsgradienten vorhanden sind.):
A. Na+
B. Na+ und Ca2+
C. Ca2+
D., K+
Ein Endplattenpotential in einer Skelettmuskelzelle könnte prinzipiell durch eine verminderte Permeabilität für welches der folgenden Ionen(n) erzeugt werden? (Nehmen wir an, dass es eine endliche anfängliche Permeabilität für jedes der unten aufgeführten Ionen gibt und dass physiologische Konzentrationsgradienten vorhanden sind.):
A. Na+ Diese Antwort ist FALSCH.
Ein Endplattenpotential ist eine Depolarisation, die normalerweise durch die gleichzeitige Erhöhung der Permeabilität für Natrium-und Kaliumionen erzeugt wird., Bei einer selektiven Abnahme der Natriumpermeabilität würde eine solche Abnahme nicht zu einer Depolarisation führen. Vielmehr würde es tatsächlich zu einer Hyperpolarisation führen, da Alpha in der GHK-Gleichung reduziert würde. Das Verhältnis der Permeabilität zu Natrium und Kalium würde in Richtung der Kaliumpermeabilität begünstigt, wobei das Membranpotential in Richtung des Kaliumgleichgewichtspotentials bewegt und eine Hyperpolarisation erzeugt würde.
B. Na+ und Ca2+
C. Ca2+
D., K+
Ein Endplattenpotential in einer Skelettmuskelzelle könnte prinzipiell durch eine verminderte Permeabilität für welches der folgenden Ionen(n) erzeugt werden? (Nehmen wir an, dass es eine endliche anfängliche Permeabilität für jedes der unten aufgeführten Ionen gibt und dass physiologische Konzentrationsgradienten vorhanden sind.):
A. Na+
B. Na+ und Ca2+ Diese Antwort ist FALSCH.
Wenn die Durchlässigkeit für Natrium und Kalzium verringert würde, wären ihre Folgen ähnlich denen in Vitamin A. Eine Verringerung der Natriumpermeabilität allein würde dazu neigen, die Zelle zu hyperpolarisieren., In ähnlicher Weise kann eine Verringerung der Calciumpermeabilität auch die Zelle hyperpolarisieren. Das Calciumgleichgewichtspotential ist ein sehr positiver Wert, und wenn es eine tonische Restpermeabilität für Calcium gäbe, würde diese Permeabilität zu einer tonischen Depolarisation des Membranpotentials beitragen. Daher würde eine Abnahme der Calciumpermeabilität diesen tonischen depolarisierenden Effekt beseitigen und zu einer Hyperpolarisation führen.
C. Ca2+
D., K+
Ein Endplattenpotential in einer Skelettmuskelzelle könnte prinzipiell durch eine verminderte Permeabilität für welches der folgenden Ionen(n) erzeugt werden? (Nehmen wir an, dass es eine endliche anfängliche Permeabilität für jedes der unten aufgeführten Ionen gibt und dass physiologische Konzentrationsgradienten vorhanden sind.):
A. Na+
B. Na+ und Ca2+
C. Ca2+ Diese Antwort ist FALSCH.
Eine Abnahme der Calciumpermeabilität allein würde, wenn überhaupt, eine Hyperpolarisation hervorrufen. Finden Sie die Logik der Antwort auf Wahl, B.
D., K+
Ein Endplattenpotential in einer Skelettmuskelzelle könnte prinzipiell durch eine verminderte Permeabilität für welches der folgenden Ionen(n) erzeugt werden? (Nehmen wir an, dass es eine endliche anfängliche Permeabilität für jedes der unten aufgeführten Ionen gibt und dass physiologische Konzentrationsgradienten vorhanden sind.):
A. Na+
B. Na+ und Ca2+
C. Ca2+
D. K+ Diese Antwort ist RICHTIG!
Eine Abnahme der Kaliumpermeabilität würde zu einer Depolarisation ähnlich einem Endplattenpotential führen., Dies ist so, weil es in Ruhe eine tonische Permeabilität für Kalium und Natrium gibt. Die hohe Kaliumpermeabilität neigt dazu, das Membranpotential in der Nähe des Kaliumgleichgewichtspotentials zu halten. Wenn diese Ruhepermeabilität verringert wird, würde Alpha in der Goldman-Gleichung zu einem größeren Wert werden und das Membranpotential ein wenig näher an das Natriumgleichgewichtspotential (dh eine Depolarisation) heranführen.