Kaliumsulfid, dargestellt durch die chemische Formel K2S, ist eine Verbindung aus Kalium und Schwefel, die in Säuren mäßig löslich ist . Es ist deliquescent und kann sich spontan in der Luft entzünden. Es ist ein Reduktionsmittel und eine ionische Verbindung .

Kaliumsulfid
Zusammensetzung und Synthese
Kaliumsulfid kann hergestellt werden, indem zuerst Kaliumhydroxid zu überschüssigem Schwefelwasserstoff unter Bildung von Kaliumhydrosulfid (KHS) behandelt wird., Die weitere Behandlung von KHS mit der gleichen Menge Kaliumhydroxid erzeugt Kaliumsulfid .,H2S = KHS + H2O
KHS + KOH = K2S + H2O

Potassium Sulfide Formula
Properties and Characteristics of Potassium Sulfide
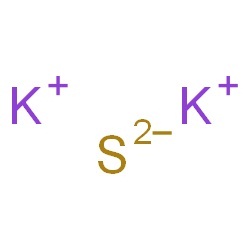
Potassium Sulfide Structure
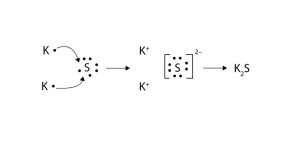
Lewis Dot Structure for Potassium Sulfide
Prominent Reactions of K2S
Potassium sulfide reacts with cobalt iii bromide to produce cobalt iii sulfide and potassium bromide .,
3K2S + 2CoBr3 = Co2S3 + 6KBr
Kaliumsulfid reagiert mit verdünnter Salzsäure zur Herstellung von Kaliumchlorid und Schwefelwasserstoff .
K2S + 2HCl = 2 KCl + H2S
Es reagiert mit konzentrierter Schwefelsäure zu Kaliumbisulfat, Schwefeldioxid, Schwefel und Wasser
K2S + 3H2SO4 = 2KHSO4 + SO2 + S + 2H20
Die Verbindung reagiert mit Silbernitrat zu wässrigem Kaliumnitrat und Silbersulfid-Niederschlag .
K2S + 2AgNO3 = 2KNO3 + Ag2S
Kalium-Sulfid Verwendet
- In der Pyrotechnik .
- Als Reagenz in der analytischen Chemie .,
- Als Enthaarungsmittel und Medizin .
Ist es gefährlich
Es kann eine Brandgefahr verursachen, daher müssen Vorsichtsmaßnahmen getroffen werden, um es nicht mit Luft in Kontakt zu bringen. In Form von Pulver oder Staub ist es explosiv. Verschlucken, Einatmen und Hautkontakt können zu schweren Verletzungen und sogar zum Tod führen. Es wirkt sich auch schädlich auf Augen und Haut aus und verursacht Augenschäden und Hautverbrennungen. Daher sollte jeder Kontakt vermieden werden. Es emittiert giftige Dämpfe, wenn es zur Zersetzung erhitzt wird . Es ist ätzender Natur und giftig für die Umwelt .
- Kaliumsulfid-Amerikanischelemente.,com
- Kaliumsulfida – Chemspider.com
- Kaliumsulfida – Pubchem.ncbi.nlm.nih.gov
- Kaliumsulfida – Chemicalbook.com
- Es K2S sauer oder basisch? – Quora.com
- Dikaliumsulfida – Webelements.com
- Was sind die Verwendungen von Kaliumsulfida? – Quora.com
- Kaliumsulfida – Merckmillipore.com
- Herstellung von Kaliumsulfida – Prepchem.com
- Löslichkeitsregeln und Net Ionischen Gleichungen Praxis – Vincentianacademy.org
- Kaliumsulfida reagieren mit Chlorwasserstoff-Chemiday.,com
- Question #e42f1 – Socratic.org
- Potassium sulfide react with sulfuric acid – Chemiday.com