Wie Sie vielleicht vom Namen erwarten, sind Superacids extrem starke Säuren, viel stärker als herkömmliche starke Mineralsäuren wie Schwefelsäure und Salzsäure.
Säure bezieht sich auf die Fähigkeit, Protonen, H+, zu anderen Substanzen hinzuzufügen: Je stärker die Säure ist, desto größer ist ihre Fähigkeit, andere Substanzen zu protonieren.
Ein Superacid ist definiert als eine Substanz, die ein höheres H+ chemisches Potential als 100% reine Schwefelsäure aufweist.,

List of Superacids
| Substance | Formula | H0 | |
|---|---|---|---|
| Chlorosulfuric acid | HSO3Cl 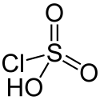 |
-12.8 | Reacts with alcohols to produce alkyl sulfate detergents. |
| Triflic acid | CF3SO3H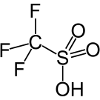 |
-14.1 | Also known as trifluoromethanesulfonic acid, or TFMS., Reagiert mit Alkoholen, um Ether und Olefine zu produzieren. |
| Oleum | H2SO4 + SO3 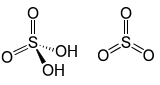 |
-15 | Schwefeltrioxid gelöst in reiner Schwefelsäure erzeugt Oleum, das über Verdünnung mit Wasser eine bevorzugte Methode zur Herstellung konzentrierter Schwefelsäure ist.Oleum wird auch als Reaktant bei der Herstellung von Sprengstoffen wie Nitrocellulose verwendet. |
| Fluorschwefelsäure | HSO3F 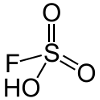 |
-15.,1 | Wird zur Herstellung von Bleisäure (siehe unten) und zur Regenerierung der HF-und H2SO4-Gemische zum Ätzen von Bleiglas verwendet. |
| Carboransäure | H (CHB11X11) |
-18.0 | Das links gezeigte Carboran ist fluoriert; chlorierte Carborane sind ebenfalls Superacide, jedoch mit geringerem Säuregehalt.Fluorierte Carboransäure ist die einzige Säure, die CO2 protonieren kann, um +zu produzieren.Carboran ist die einzige Säure, die C60 ohne Nebenreaktionen protonieren kann.Carboranprotonate Benzol C6H7+ Salz zu ergeben.,Obwohl sie eine große protonisierende Kraft haben, sind Carborane weniger ätzend als andere Superacids; Im Gegensatz zu den meisten können sie in einer Glasflasche gelagert werden. |
| Magic acid | FSO3H·SbF5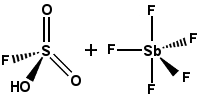 |
-19.2 | Vorbereitet von fluorosulfuric Säure (siehe oben) – und Antimon-pentafluoride. Katalysiert die Isomerisierung gesättigter Kohlenwasserstoffe, stabilisiert Carbokationen. |
| Fluorantimonsäure | H2FSbF6 oder H2F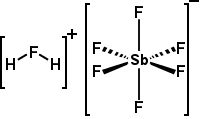 |
-31.,3 | Das stärkste Superacid, es wird durch Reaktion eines 2:1 Molverhältnisses von HF mit SbF5 erzeugt. Kann fast jede organische Verbindung protonieren. |
Der Säuregehalt wird durch die Hammett-Säurefunktion H0 angezeigt.
Wie der pH-Wert ist H0 ein Maß für den Säuregehalt; niedrigere Werte von H0 bedeuten eine höhere Protonierleistung.Wie pH ist H0 eine logarithmische Skala.
100% Schwefelsäure hat einen H0 von -12.Vergleichen Sie dies mit Fluorantimonsäure H0 von -31.Dies bedeutet, dass Fluorantimonsäure 1019 saurer ist als reine Schwefelsäure., Das ist ein größerer Unterschied als zwischen der Größe der Sonne und der Größe einer Amöbe.
