Osmose
Stellen Sie sich nun vor, Sie haben eine zweite Tasse mit \(100 \: \text{mL}\) Wasser und fügen dem Wasser \(45 \: \text{g}\) Tafelzucker hinzu. Genau wie die erste Tasse ist der Zucker der gelöste und das Wasser das Lösungsmittel. Aber jetzt haben Sie zwei Mischungen mit unterschiedlichen gelösten Konzentrationen. Beim Vergleich von zwei Lösungen mit ungleicher gelöster Konzentration ist die Lösung mit der höheren gelösten Konzentration hypertonisch und die Lösung mit der niedrigeren gelösten Konzentration hypoton., Lösungen gleicher gelöster Konzentration sind isotonisch. Die erste Zuckerlösung ist hypotonisch zur zweiten Lösung. Die zweite Zuckerlösung ist hypertonisch zur ersten.
Sie fügen nun die beiden Lösungen einem Becher hinzu, der durch eine semipermeable Membran geteilt wurde, mit Poren, die zu klein sind, um die Zuckermoleküle zu passieren, aber groß genug sind, um die Wassermoleküle zu passieren. Die hypertonische Lösung ist eine Seite der Membran und die hypotonische Lösung auf der anderen., Die hypertonische Lösung hat eine niedrigere Wasserkonzentration als die hypotonische Lösung, so dass jetzt ein Konzentrationsgradient von Wasser über die Membran existiert. Wassermoleküle bewegen sich von der Seite der höheren Wasserkonzentration zur Seite der niedrigeren Konzentration, bis beide Lösungen isotonisch sind. An diesem Punkt ist das Gleichgewicht erreicht.
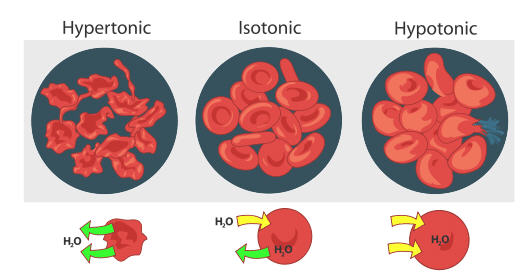
Rote Blutkörperchen verhalten sich gleich (siehe Abbildung unten). Wenn sich rote Blutkörperchen in einer hypertonischen Lösung (höhere Konzentration) befinden, fließt Wasser schneller aus der Zelle als es hereinkommt. Dies führt zu einer Crenation (Shriveling) der Blutzelle., Auf der anderen Seite führt ein hypotonisches rotes Blutkörperchen (niedrigere Konzentration außerhalb der Zelle) dazu, dass mehr Wasser in die Zelle fließt als heraus. Dies führt zu einer Schwellung der Zelle und einer möglichen Hämolyse (Platzen) der Zelle. In einer isotonischen Lösung geschieht der Wasserfluss in und aus der Zelle mit der gleichen Geschwindigkeit.
Osmose ist die Diffusion von Wassermolekülen über eine semipermeable Membran von einem Bereich mit einer niedrigeren Konzentrationslösung (dh einer höheren Konzentration von Wasser) zu einem Bereich mit einer höheren Konzentrationslösung (dh einer niedrigeren Konzentration von Wasser). Wasser bewegt sich in und aus den Zellen durch Osmose.
- Wenn sich eine Zelle in einer hypertonischen Lösung befindet, hat die Lösung eine niedrigere Wasserkonzentration als das Zellzytosol und Wasser bewegt sich aus der Zelle, bis beide Lösungen isotonisch sind.,
- Zellen, die in eine hypotonische Lösung gegeben werden, nehmen Wasser über ihre Membranen auf, bis sowohl die äußere Lösung als auch das Cytosol isotonisch sind.
Ein roter Blutkörperchen schwillt an und unterzieht sich einer Hämolyse (Burst), wenn er in eine hypotonische Lösung gegeben wird. Wenn eine rote Blutkörperche in eine hypertonische Lösung gegeben wird, verliert sie Wasser und unterzieht sich einer Crenation (Shrivel). Tierische Zellen neigen dazu, am besten in einer isotonischen Umgebung zu tun, wo der Fluss von Wasser in und aus der Zelle mit gleichen Raten auftritt.