Lewis struktur av vattenmolekylen innehåller två enkelbindningar runt syreatom. antal totala valenselektroner av syre och väteatomer används för att rita lewis struktur. Varje steg för att dra lewis struktur H2O förklaras i denna handledning.
H2o lewis struktur
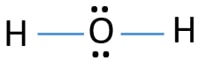
i lewis struktur H2O, det finns två enkla bindningar runt syre atom. Väteatomer är gemensamma för syreatom genom enskilda bindningar. Det finns också två ensamma par på syreatom.,
vattenmolekyl är en enkel molekyl. Ritning lewis struktur av vattenmolekyl är enkel än några av andra komplexa molekyler eller joner. Tänk dig att dra lewis struktur av tiosulfatjon.
steg för att rita lewis struktur av H2O
det finns några steg att följa för att rita en lewis struktur ordentligt. För H2o molekyl, dess lewis struktur och dessa steg förklaras i detalj i denna handledning. Eftersom vattenmolekylen är enkel, används några av dessa steg inte mycket. I sådana fall nämns de med respektive steg.,
- hitta Totalt antal elektroner av valansskal av väteatomer och syreatom
- totala elektroner par som ensamstående par och bindningar
- Center atom val
- markera ensamstående par på atomer
- markera laddningar på atomer om det finns.
- kontrollera stabiliteten och minimera laddningar på atomer genom att konvertera ensamstående par till bindningar för att få bästa lewis struktur.
viktigt: ritning korrekt lewis struktur är viktigt att dra resonans strukturer korrekt.,
Totalt antal elektroner av ventilationsskalorna i H2O
det finns två av elementen; väte och syre. Väte är ett grupp IA-element och har bara en elektron i sitt sista skal (valence shell). Syre är en grupp VIA element i det periodiska systemet och innehåller sex elektroner i sitt sista skal. Nu vet vi hur många elektroner som ingår i valensskal av varje atom.,
- valenselektroner som ges av väteatomer = 1 * 2 = 2
- valenselektroner som ges av syreatomer = 6*1 = 6
- totala valenselektroner = 2 + 6 = 8
totala valenselektroner par
totala valenselektroner par = σ bindningar + π bindningar + lone par vid valensskal
totala valenselektroner par = σ bindningar + π bindningar + lone par p >
totala elektronpar bestäms genom att dividera antalet totala valenselektroner med två. För, H2O, är totala par elektroner 4 i sina valensskal.,
Center atom av H2O
för att vara Center atom, förmåga att ha större valans är viktigt. Sedan, från väte och syre, vilken atom har den högsta valensen? Maximal syrevalens är två. vätgas enda valens är en. Därför bör syreatomen vara H2O: s mittatom. nu kan vi rita en skiss av H2O för att visa hur atomer finns i molekylen.
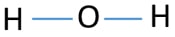
Lone pairs on atoms
efter bestämning av Center atom och skiss av H2o molekyl, bör vi börja markera lone pairs on atoms., Kom ihåg att det finns totalt fyra elektronpar.
- Det finns redan två H-O-bindningar i den ritade skissstrukturen. Nu återstår bara två (4-2) elektronpar för att markera på atomer.
- vanligtvis bör de återstående elektronpar börja markera på yttre atomer. Men i H2O är väteatomen de yttre atomer som inte kan hålla mer än två elektron i sitt sista skal. Därför kan vi inte markera dessa två elektroner par på väteatomer.,
- markera sedan de två elektronpar på mittatom; syre

markera laddningar på atomer
det finns inga laddningar på syreatom och väteatomer.
kontrollera stabiliteten och minimera laddningar på atomer genom att konvertera ensamma par till bindningar
eftersom det inte finns några laddningar på atomer, behöver du inte minska laddningarna som ett steg för att dra bästa lewis struktur. Redan, vi fick den bästa lewis struktur för H2O.
frågor
vilka är de liknande lewis strukturer till vatten kan dras för?,
i lewis struktur av vattenmolekyl, det finns två sigma bindningar och två ensamma par runt sulfuratom. Vätesulfid, syredifluorid (F2O) har liknande lewis strukturer till vatten.
Ställ dina Kemi frågor och hitta svaren
relaterade Tutorials