Lewis structure of water molecule contains two single bonds around oxygen atom. número total de elétrons de valência de átomos de oxigênio e hidrogênio são usados para desenhar a estrutura de lewis. Cada passo de desenho de lewis estrutura de H2O são explicados neste tutorial.
H2o lewis structure
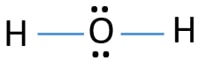
In The lewis structure of H2O, there are two single bonds around oxygen atom. Átomos de hidrogênio são comuns ao átomo de oxigênio através de ligações únicas. Além disso, há dois pares solitários no átomo de oxigénio.,
a molécula de água é uma molécula simples. Desenhar a estrutura de lewis da molécula de água é simples do que algumas outras moléculas complexas ou íons. Imagine desenhar a estrutura de lewis do íon tiossulfato.
Steps of drawing lewis structure of H2O
There are some steps to follow to draw a lewis structure properly. Para a molécula de H2o, sua estrutura de lewis e esses passos são explicados em detalhes neste tutorial. Como a molécula de água é simples, alguns desses passos não são usados muito. Nesses casos, são mencionados com as respectivas etapas.,
- encontrar o número total de electrões das camadas de Valência dos átomos de hidrogénio e do átomo de oxigénio
- total de electrões pares como pares isolados e ligações
- selecção do átomo central
- marcar as cargas nos átomos se existirem.
- Verifique a estabilidade e minimize as cargas nos átomos, convertendo pares solitários em ligações para obter a melhor estrutura de lewis.
marcar os pares isolados nos átomos
importante: desenhar a estrutura correcta de lewis é importante para desenhar as estruturas de ressonância correctamente.,
número Total de electrões das camadas de valência da H2O
Existem dois elementos: hidrogénio e oxigénio. O hidrogênio é um elemento do grupo IA e tem apenas um elétron em sua última concha (concha de Valência). O oxigênio é um grupo VIA elemento na tabela periódica e contém seis elétrons em sua última concha. Agora sabemos quantos elétrons estão incluídos em conchas de valência de cada átomo.,
- elétrons de valência dada por átomos de hidrogênio = 1 * 2 = 2
- elétrons de valência dada por átomos de oxigênio = 6*1 = 6
- Total de elétrons de valência = 2 + 6 = 8
Total de elétrons de valência pares
Total de valência elétrons pares = σ obrigações + π obrigações + solitário pares, em valência conchas
Total de pares de elétrons são determinados dividindo-se o número total de elétrons de valência por dois. Para, H2O, pares totais de elétrons são 4 em suas conchas de Valência.,
átomo central de H2O
para ser o átomo central, a capacidade de ter maior valância é importante. Então, a partir de hidrogênio e oxigênio, qual átomo tem a mais alta Valência? A valência máxima do oxigénio é de dois. a única valência do hidrogénio é uma. Portanto, átomo de oxigênio deve ser o átomo central de H2O. agora, podemos desenhar um esboço de H2O para mostrar como os átomos estão localizados na molécula.
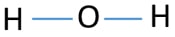
pares solitários em átomos
Depois de determinar o átomo central e esboço da molécula de H2O, devemos começar a marcar pares solitários em átomos., Lembre-se disso, há um total de quatro pares de elétrons.
- já existem duas obrigações H-O na estrutura esboçada. Agora apenas dois pares de elétrons (4-2) permanecem para marcar nos átomos.geralmente, esses pares de elétrons remanescentes devem ser iniciados para marcar em átomos externos. Mas em H2O, átomo de hidrogênio são os átomos externos que não podem manter mais de dois elétrons em sua última concha. Portanto, não podemos marcar esses dois elétrons pares em átomos de hidrogênio.,
- ntão, marque esses dois elétrons pares no átomo central; oxigênio

marque cargas nos átomos
não há cargas no átomo de oxigênio e hidrogênio.
Verifique a estabilidade e minimize as cargas nos átomos, convertendo pares solitários em ligações
porque não há cargas nos átomos, não há necessidade de reduzir as cargas como um passo de desenhar a melhor estrutura de lewis. Já temos a melhor estrutura de lewis para H2O.
Questions
quais são as estruturas de lewis similares à água que podem ser desenhadas?,
na estrutura de lewis da molécula de água, existem duas ligações sigma e dois pares solitários em torno de sulfuratomáceas. Sulfeto de hidrogênio, Difluoreto de oxigênio (F2O) tem estruturas de lewis similares à água.
faça as suas perguntas de química e encontre as respostas tutoriais relacionadas