Heat and temperature are a closely related topic, and as such, the difference between the two can be a bit confusing. A diferença fundamental é que o calor lida com a energia térmica, enquanto a temperatura está mais preocupada com a energia cinética molecular.
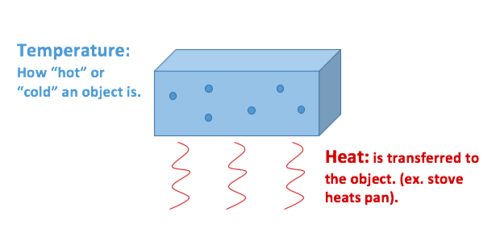
Calor é a transferência de energia térmica, enquanto que a temperatura é uma propriedade do objeto de exposições.
Qual é a diferença?,
calor descreve a transferência de energia térmica entre moléculas dentro de um sistema e é medida em Joules. O calor mede como a energia se move ou flui. Um objeto pode ganhar calor ou perder calor, mas não pode ter calor. O calor é uma medida de mudança, nunca uma propriedade possuída por um objeto ou sistema. Portanto, é classificado como uma variável de processo.
temperatura descreve a energia cinética média das moléculas dentro de um material ou sistema e é medida em Celsius (°C), Kelvin(K), Fahrenheit (°F), ou Rankine (R)., É uma propriedade física mensurável de um objeto—também conhecida como uma variável de Estado. Outras propriedades físicas mensuráveis incluem velocidade, massa e densidade, para citar algumas.
semelhanças
calor é uma transferência de energia térmica causada por uma diferença de temperatura entre moléculas.Nota: A energia térmica pode ser entendida como a energia cinética e potencial total microscópica de um sistema.,
Segunda Lei da Termodinâmica
A segunda lei da termodinâmica é um tema complexo que requer estudo intensivo no campo da termodinâmica, para entender verdadeiramente. No entanto, para efeitos deste artigo, apenas um pequeno aspecto precisa de ser compreendido e é o facto de o calor fluir sempre espontaneamente de substâncias mais quentes para substâncias mais frias. Esta simples declaração explica por que um cubo de gelo não se forma fora em um dia quente ou por que ele derrete quando cair em uma tigela de água quente.,Imagine o acima mencionado cubo de gelo caído em uma bacia de água quente—o gelo deve ganhar calor (energia térmica) a partir da água na bacia (ver parágrafo anterior). A adição de energia térmica leva a um aumento na energia cinética da molécula de gelo, e, portanto, um aumento na temperatura. Isto é conhecido porque a temperatura é de fato a medida da energia cinética média das moléculas. Além disso, o gelo continuará a ganhar energia térmica fazendo com que suas moléculas se movam mais rápido e eventualmente quebrem suas ligações intermoleculares ou derretam., em conclusão, a transferência de calor ou energia térmica normalmente altera a temperatura da substância, mas nem sempre! Por exemplo, no momento em que o gelo na bacia se transforma em água essas moléculas de água estarão exatamente à mesma temperatura que quando eram gelo. Neste caso, em vez da energia térmica que trabalha para aumentar a energia cinética, ela trabalha para quebrar as ligações intermoleculares, causando uma mudança de Estado., No entanto, com o passar do tempo, a temperatura do gelo derretido recentemente vai aumentar até que tudo dentro da tigela atinja o equilíbrio—o que significa uma temperatura consistente ao longo.
Para Ler Mais
- Calor
- Temperatura
- energia Térmica
- energia Cinética
- energia Interna
- Ou explorar uma página aleatória