jak można się spodziewać po nazwie, superacydy są niezwykle silnymi kwasami, znacznie silniejszymi niż tradycyjne silne kwasy mineralne, takie jak kwas siarkowy i kwas solny.
kwasowość odnosi się do zdolności do dodawania protonów, H+, do innych substancji: im silniejszy kwas, tym większa jego moc do protonowania innych substancji.
superacyd jest zdefiniowany jako substancja o wyższym potencjale chemicznym H+ niż 100% Czysty Kwas siarkowy.,

List of Superacids
| Substance | Formula | H0 | |
|---|---|---|---|
| Chlorosulfuric acid | HSO3Cl 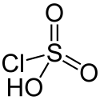 |
-12.8 | Reacts with alcohols to produce alkyl sulfate detergents. |
| Triflic acid | CF3SO3H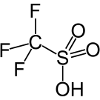 |
-14.1 | Also known as trifluoromethanesulfonic acid, or TFMS., Reaguje z alkoholem, tworząc etery i olefiny. |
| Oleum | H2SO4 + SO3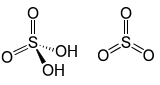 |
-15 | tritlenek siarki rozpuszczony w czystym kwasie siarkowym wytwarza oleum, który jest preferowaną metodą, poprzez rozcieńczenie wodą, wytwarzania stężonego kwasu siarkowego.Oleum jest również stosowany jako reagent w produkcji materiałów wybuchowych, takich jak nitroceluloza. |
| kwas Fluorosulfurowy | HSO3F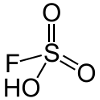 |
-15.,1 | jest używany do przygotowania kwasu magicznego (patrz poniżej) i do regeneracji mieszanin HF i H2SO4 stosowanych do wytrawiania szkła ołowiowego. |
| kwas Karboranowy | H(CHB11X11) |
-18.0 | karboran pokazany po lewej stronie jest fluorowany; chlorowane karborany są również nadkwasotami, ale o niższej kwasowości.Fluorowany kwas karboranowy jest jedynym kwasem zdolnym do protonowania CO2 w celu wytworzenia +.Karboran jest jedynym kwasem zdolnym do protonowania C60 bez reakcji ubocznych.Karboran protonizuje benzen w celu uzyskania soli C6H7+.,Chociaż mają dużą moc protonowania, karborany są mniej żrące niż inne superacydy; w przeciwieństwie do większości, mogą być przechowywane w szklanej butelce. |
| kwas magiczny | fso3h·SbF5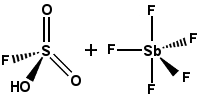 |
-19.2 | przygotowany z kwasu fluorosulfurowego (patrz wyżej) i pentafluorku antymonu. Katalizuje izomeryzację nasyconych węglowodorów, stabilizuje węglowodory. |
| kwas Fluoroantimonowy | H2FSbF6 lub H2F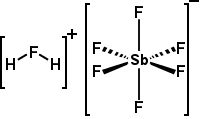 |
-31.,3 | najpotężniejszy superacyd, jest wytwarzany przez reakcję w stosunku molowym HF 2: 1 z SbF5. Może protonować prawie każdy związek organiczny. |
kwasowość jest wskazywana przez funkcję kwasowości Hammetta, H0.
podobnie jak pH, H0 jest miarą kwasowości; niższe wartości H0 oznaczają wyższą moc protonowania.Podobnie jak pH, H0 jest skalą logarytmiczną.
100% Kwas siarkowy ma H0 od -12.Porównaj to z H0 kwasu fluoroantimonowego z -31.Oznacza to, że kwas fluoroantimonowy jest o 1019 bardziej kwaśny niż czysty kwas siarkowy., To większa różnica między wielkością słońca a wielkością ameby.
