Hva er et Ion?
Et ion er et atom eller molekyl som bærer en elektrisk ladning.
Ioner er identifisert ved bruk av en hevet til å vise fortegnet og størrelsen av deres elektrisk ladning.
Anioner og Kationer
Negativt ladede ioner kalles anioner, og positivt ladede ioner kalles kationer.,n atom gevinster tre elektroner til å bli N3-
Eksempler på Kationer
- en sodium atom mister et elektron til å bli Na+
- en magnesium atom mister to elektroner til å bli Mg2+
- et strykejern atom mister tre elektroner til å bli Fe3+
- vann reagerer med H+ for å danne den molekylære cation H3O+
– Ion-Formasjon
Ioner form når du gjør dette reduserer den totale potensielle energi i kjemiske arter som er involvert i en kjemisk reaksjon.,Ofte er dette oppnås ved at atomer av ulike elementer for å oppnå et fullt skall av elektroner.
Vurdere salt litium fluor:
Litium-atomer har 3 elektroner, noe som betyr at de har elektroner i to skall: 2 i den første shell og 1 i second.By å miste et elektron til å bli et kation, litium får en stabil electron arrangement, identisk med den edle gass helium.,
Li Atom
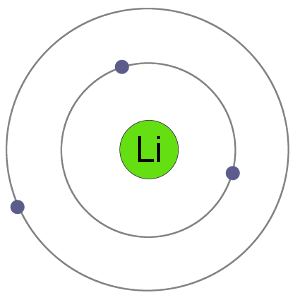
Li+ Cation
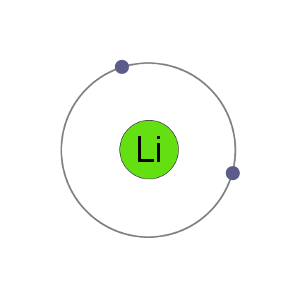
Fluor atomene har 9 elektroner, noe som betyr at de har 2 i den første shell og 7 i second.By å få et elektron til å bli et anion fluor ion får en stabil electron arrangement, identisk med den edle gass neon.,»e9c2d99c83″>
Og så redoks-reaksjon av natrium med klor for å danne en ionisk forbindelsen er energetisk gunstig:
Reduksjon av klor: Cl2 + 2e- → 2Cl-
Generelle reaksjon: 2Na + Cl2 → 2NaCl
– Ion-Størrelser
Kationer er mindre enn den opprinnelige atom – vurdere hvordan sodium atom har elektroner i tre skjell, mens natrium ion har elektroner i bare to skjell.,Med flere elektroner, anioner er større enn den opprinnelige atom.
Ion-størrelser måles ved det ioniske radius.
Ioniske Radier i Picometers
Den grå fargen i diagrammer viser størrelsen på originalen atom. Den blå (kation) og gul (anion) viser størrelsen av ion. (Diagrammer av Chris King.)

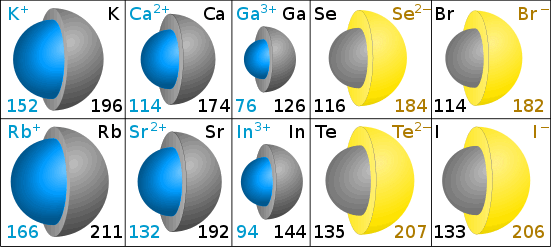
Ioniske Forbindelser
Ioniske forbindelser, som for eksempel natriumklorid (NaCl) er dannet på grunn av elektrostatisk tiltrekning mellom anioner og kationer.,Ioniske forbindelser er elektrisk nøytral, fordi det totale antall positive avgifter, og det totale antall negative ladninger er alltid lik.
Vurderer kjemiske elementer, den høyeste tendens til å danne ioniske forbindelser finnes i minst electronegative metaller og de mest electronegative ikke-metaller.
Elektriske Ledere
Ioner kan bære elektrisk strøm, og dette kan observeres i elektrokjemiske celler, og i plasma, for eksempel.
generelt, solid ioniske forbindelsene ikke bære elektrisk strøm, fordi ionene er låst i faste posisjoner i en krystall gitter.,Ioniske forbindelser bare elektrisitet når smeltet eller når det løses i løsningen, når ioner frigjøres fra crystal gitter og bli mobile.