生物学的療法には、幅広い医療製品が含まれています。 ワクチン、血液製剤、および幹細胞注射は、第一世代の生物学的療法の例である。 しかし、人々が”生物製剤”について話すとき、彼らは通常、Humira、Remicade、およびEnbrelなどの第二世代の生物学的治療薬を意味します。
RAおよびその他の自己免疫状態に関する生物学的応答修飾剤は、関節リウマチおよび強直性脊椎炎などの炎症性自己免疫疾患を治療するために, 生物製剤を読む:患者のための基本的な事実
生物学的療法(第一および第二世代の両方)は、実験室で成分を一緒に混合するなど、単純な化学反応を用いて行うことはできない、従来の薬物が作られる方法。 代わりに、生物学的療法は、細菌、酵母、さらには哺乳動物の組織および細胞などの生きた生物を使用して行われる。
生物製剤の製造
生物製剤は、生きた細胞を含む非常に複雑な製造プロセスを使用して製造されます。,
製造方法はさまざまですが、炎症性関節痛を治療するために今日販売されているほとんどの生物製剤は、次の基本的なステップを使用して製造されます。
- DNAの一部が生きている細胞、すなわち酵母、細菌、ウイルス、または哺乳類細胞に挿入されます。
- DNAの断片は、大量の特定の分子、通常はタンパク質を産生するように細胞に指示する。
- その後、分子が単離され、生きている細胞および他の物質がなくなり、所望の分子のみが残される。
- 単離された分子は、生物学的薬物中の活性成分となる。,
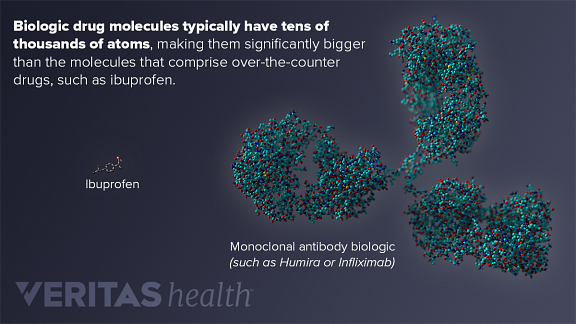
生物学的薬物中の分子は、その大きなサイズ、均一性の欠如、および弱い化学結合のために、他のほとんどの医薬品の分子とは異なります。
大きなサイズと均一性の欠如
生物学的薬物を構成する分子は一様に同じではなく、各分子は典型的には数万原子を持っています。弱い化学結合
これらの分子を一緒に保持する化学結合は比較的弱い。 それらが急速な温度変化および他の要因にさらされると、分子は分解する可能性があります。,生物学的製剤を構成する分子は非常に敏感であるため、製造業者は生物学的製剤を製造して包装する特定の手順に従わなければならない。 生物学的製造および包装プロセス、ならびに貯蔵および投与のわずかな違いでさえ、薬物の作用能力に影響を及ぼす可能性がある。
 保存
保存生物製剤のFDA承認
FDAが従来の薬物を承認すると、それはそれが含まれているどのように多くの炭素原, このタイプの評価は、生物製剤では行うことができません:それらの分子の変化と大きなサイズは、研究者が生物製剤中のすべての分子を分析し、正確に記述することを不可能にします。
生物製剤のリスクと副作用を参照してください
広告生物製剤は特徴付けるのが難しいため、生物製剤のFDA承認はその製造プロセスに基づいています。 FDAは、最終製品が一貫していることを確認するためにプロセスをレビューし、あるバッチと別のバッチの間に大きな変動はありません。, 生物製剤評価および研究センター(CBER)は、生物製剤の安全性および有効性を確保する責任があります。