化学式K2Sで表される硫化カリウムは、酸に適度に可溶性であるカリウム それは潮解性であり、空気中で自発的に発火する可能性があります。 それは還元剤およびイオン性化合物である。

硫化カリウム
組成および合成
硫化カリウムは、まず水酸化カリウムを過剰な硫化水素に処理して硫化カリウム(KHS)を形成することによって調製することができる。, 同じ量の水酸化カリウムでKHSをさらに処理すると、硫化カリウムが生成されます。,H2S = KHS + H2O
KHS + KOH = K2S + H2O

Potassium Sulfide Formula
Properties and Characteristics of Potassium Sulfide
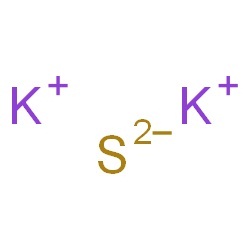
Potassium Sulfide Structure
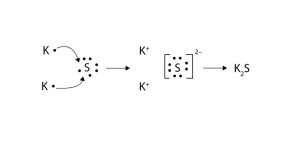
Lewis Dot Structure for Potassium Sulfide
Prominent Reactions of K2S
Potassium sulfide reacts with cobalt iii bromide to produce cobalt iii sulfide and potassium bromide .,
3K2S+2CoBr3=Co2S3+6KBr
硫化カリウムは希塩酸と反応して塩化カリウムと硫化水素を生成する。
K2S+2HCl=2KCl+H2S
濃硫酸と反応して重硫酸カリウム、二酸化硫黄、硫黄および水を得る
K2S+3H2SO4=2KHSO4+SO2+S+2H20
化合物は硝酸銀と反応して硝酸カリウム水溶液および硫化銀沈殿物を形成する。
K2S+2AgNO3=2KNO3+Ag2S
硫化カリウムは花火に
- を使用します。
- 分析化学における試薬として。,
- 脱毛と薬として。li>
それは危険ですか
火災の危険を引き起こす可能性がありますので、空気と接触させないように注意する必要があります。 粉または塵の形で、それは爆発性である。 摂取、吸入および皮膚の接触は厳しい傷害および死で起因するかもしれません。 それはまた有害に目に影響を与え、目の損傷および皮の焼跡を引き起こす皮。 よって、全ての接触は回避しなければならない。 それは分解に熱されたら有毒な発煙を出します。 それは環境のために腐食性の性質そして有害です。
- 硫化カリウム-アメリカ元素。,com
- 硫化カリウム–Chemspider.com
- 硫化カリウム–Pubchem.ncbi.nlm.nih.gov
- 硫化カリウム–Chemicalbook.com
- それはK2S酸性または塩基性ですか? –Quora.com
- 硫酸二カリウム–Webelements.com li>
- 硫化カリウムの用途は何ですか? –Quora.com
- 硫化カリウム–Merckmillipore.com
- 硫化カリウムの調製–Prepchem.com
- 溶解度ルールとネットイオン方程式の練習–Vincentianacademy.org
- 硫化カリウムは塩化水素と反応する。,com
- Question #e42f1 – Socratic.org
- Potassium sulfide react with sulfuric acid – Chemiday.com