Figura 4.1 (vedere visualizzazione ingrandita)
di Conseguenza, la comprensione di questo sinapsi che conduce alla comprensione degli altri. Pertanto, discuteremo prima il processo di trasmissione sinaptica alla giunzione neuromuscolare scheletrica.,
Le caratteristiche della giunzione sinaptica alla giunzione neuromuscolare sono mostrate nella figura a sinistra. Le fibre muscolari scheletriche sono innervate dai motoneuroni i cui corpi cellulari si trovano nel corno ventrale del midollo spinale. La regione terminale dell’assone dà origine a processi molto fini che corrono lungo le cellule muscolari scheletriche. Lungo questi processi sono strutture specializzate note come sinapsi. La particolare sinapsi fatta tra un motoneurone spinale e la cellula muscolare scheletrica è chiamata piastra terminale del motore a causa della sua struttura specifica.,
La sinapsi alla giunzione neuromuscolare ha tre caratteristiche caratteristiche delle sinapsi chimiche nel sistema nervoso. Innanzitutto, c’è una netta separazione tra la membrana presinaptica e la membrana postsinaptica. Lo spazio tra i due è noto come fessura sinaptica. Lo spazio ci dice che ci deve essere un meccanismo di segnalazione intermedio tra il neurone presinaptico e il neurone postsinaptico per avere un flusso di informazioni attraverso la fessura sinaptica. In secondo luogo, c’è una caratteristica alta densità di piccole vescicole sferiche., Queste vescicole sinaptiche contengono sostanze neurotrasmettitori. Le sinapsi sono anche associate ad un’alta densità di mitocondri. Terzo, nella maggior parte dei casi, c’è un ispessimento caratteristico della membrana postsinaptica, che è dovuto almeno in parte al fatto che la membrana postsinaptica ha un’alta densità di recettori specializzati che legano le sostanze chimiche del trasmettitore rilasciate dal neurone presinaptico. Ulteriori dettagli sulle caratteristiche morfologiche delle giunzioni sinaptiche sono forniti nel capitolo 8 e nel capitolo 10.
4.,2 Fisiologia della Trasmissione Sinaptica, la Giunzione Neuromuscolare
Figura 4.2
La figura a destra illustra in modo molto schematico modo in cui è possibile studiare la fisiologia della trasmissione sinaptica alla giunzione neuromuscolare scheletrica in grande dettaglio. Un pezzo di muscolo e il suo nervo attaccato sono posti in una piccola camera sperimentale riempita con una soluzione di suoneria appropriata. Il potenziale di riposo della cellula muscolare viene registrato con un microelettrodo. Gli elettrodi sono anche posizionati sulla superficie dell’assone nervoso., Brevi scosse elettriche causano l’avvio di potenziali d’azione, che si propagano al terminale sinaptico.
La figura seguente illustra due tipi di potenziali cambiamenti che sono stati registrati in una preparazione nervo-muscolo così isolata. L’esperimento illustra anche le proprietà di un potente farmaco, curare, che si è dimostrato molto utile nello studio del processo di trasmissione sinaptica alla giunzione neuromuscolare scheletrica. La parte A illustra la sequenza di potenziali cambiamenti registrati nella cellula muscolare come risultato della stimolazione dell’assone motore., La freccia indica il punto nel tempo in cui l’ammortizzatore viene consegnato all’assone del motore. Si noti che c’è un periodo di riposo dopo lo shock. Il ritardo è dovuto al tempo necessario affinché il potenziale d’azione nell’assone motore si propaghi dal suo sito di iniziazione. Dopo il ritardo, ci sono due tipi di potenziali registrati nella cellula muscolare. Innanzitutto, c’è un potenziale di cambiamento relativamente lento che sarà al centro della seguente discussione., Se quel potenziale iniziale lento è sufficientemente grande, come è normalmente nelle cellule muscolari scheletriche, un secondo potenziale, un potenziale d’azione, è suscitato nella cellula muscolare.
Figura 4.3
I potenziali d’azione nelle cellule muscolari scheletriche sono dovuti a meccanismi ionici simili a quelli discussi in precedenza. Nello specifico, c’è una variazione tensione-dipendente nella permeabilità Na+ seguita da un aumento ritardato della permeabilità K+. (Per le cellule muscolari lisce e le cellule muscolari cardiache i meccanismi ionici sono diversi, tuttavia.,)
L’evento sottostante che innesca il potenziale d’azione può essere rivelato approfittando del curaro, un veleno di freccia usato da alcuni indiani sudamericani. Una bassa dose di curaro (Parte B) riduce l’evento sottostante, ma non è ancora sufficientemente ridotta per scendere al di sotto della soglia. Se viene erogata una dose leggermente più alta di curaro (Parte C), l’evento sottostante lento diventa sottosoglia. Il segnale sottostante è noto come potenziale endplate (EPP) perché è un cambiamento potenziale registrato alla piastra terminale del motore. Generalmente, è noto come potenziale postsinaptico eccitatorio (EPSP).,
Il curaro blocca il potenziale della piastra terminale perché è un inibitore competitivo dell’acetilcolina (ACh), il trasmettitore rilasciato al terminale presinaptico. Curaro non blocca la conduttanza Na+ tensione-dipendente o la conduttanza K + tensione-dipendente che è alla base del potenziale d’azione muscolare. Il curaro influenza lo stimolo (l’EPSP) che normalmente porta all’avvio del potenziale d’azione muscolare. Un animale avvelenato con curaro asfissierà perché il processo di trasmissione neuromuscolare ai muscoli respiratori è bloccato.,
Normalmente, la grandezza del potenziale della piastra terminale è abbastanza grande. Infatti, l’ampiezza del potenziale endplate è di circa 50 mV, ma solo circa 30 mV è necessario per raggiungere la soglia. L’extra 20 mV è chiamato fattore di sicurezza. Pertanto, anche se il potenziale della piastra terminale dovesse diventare un po ‘ più piccolo (ad esempio, 40 mV in ampiezza) a causa della fatica, l’EPP raggiungerebbe la soglia e la relazione uno-a-uno tra un potenziale d’azione nell’assone motore e un potenziale d’azione nella cellula muscolare sarebbe preservata.
Figura 4.4
4.,3 Propagazione dell’EPP
Quali sono le proprietà dell’EPP e come si confronta con le proprietà del potenziale d’azione?
Il potenziale della piastra terminale è dovuto a un cambiamento dipendente dalla tensione nelle permeabilità Na+ e K+ come il potenziale d’azione?
Il potenziale endplate è propagato in modo tutto o niente come il potenziale d’azione?
La figura a sinistra illustra un esperimento che esamina la propagazione del potenziale endplate. La fibra muscolare viene impalata ripetutamente con elettrodi a intervalli di 1 mm., (Si noti che il potenziale della piastra terminale è piccolo perché questo esperimento è fatto in presenza di una bassa concentrazione di curaro, quindi il potenziale della piastra terminale può essere registrato senza le complicazioni di innescare un potenziale d’azione.) Il potenziale endplate non viene propagato in modo tutto o niente. Si diffonde lungo il muscolo, ma lo fa con decremento., Pertanto, la diffusione del potenziale endplate dal suo sito di iniziazione ad altri siti lungo la cellula muscolare avviene passivamente e con decremento, proprio come un cambiamento potenziale di sottosoglia in una porzione dell’assone si diffonde lungo l’assone, o semplicemente come un cambiamento di temperatura in un punto su un’asta metallica si diffonde lungo l’asta.
4.4 Panoramica della Sequenza di Eventi Sottostante il PPE
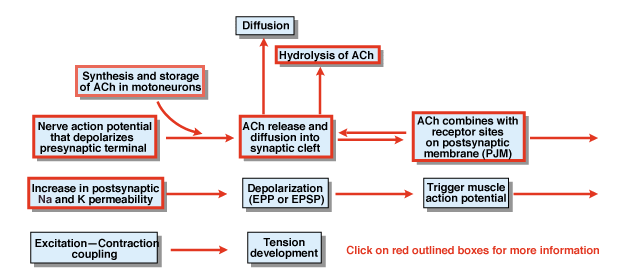
Figura 4.5
Quali sono le altre fasi del processo di trasmissione sinaptica chimica? Figura 4.,5 fornisce una panoramica. Un potenziale d’azione nervosa che viene avviato nel corpo cellulare di un motoneurone spinale propaga le radici ventrali e alla fine invade i terminali sinaptici dei motoneuroni. Come risultato del potenziale d’azione, il trasmettitore chimico acetilcolina (ACh) viene rilasciato nella fessura sinaptica. ACh si diffonde attraverso la fessura sinaptica e si lega a speciali recettori sulla membrana postsinaptica o postjunctional. Il legame di ACh ai suoi recettori produce un cambiamento conformazionale in un canale di membrana che è specificamente permeabile sia a Na+ che a K+., Come risultato di un aumento della permeabilità Na+ e K+, c’è una depolarizzazione della membrana postsinaptica. Quella depolarizzazione è chiamata potenziale di endplate o più in generale EPSP. Se l’EPSP è sufficientemente grande, come normalmente è alla giunzione neuromuscolare, porta all’avvio di un potenziale d’azione nella cellula muscolare. Il potenziale d’azione avvia il processo di accoppiamento di contrazione di eccitazione e lo sviluppo della tensione. La durata del potenziale endplate è di circa 10 msec.
Due fattori controllano la durata dell’EPSP alla giunzione neuromuscolare., Innanzitutto, ACh viene rimosso per diffusione. In secondo luogo, una sostanza nella fessura sinaptica, chiamata acetilcolinesterasi (AChE), idrolizza o scompone ACh. AChE è uno degli enzimi più efficienti conosciuti. Una singola molecola di AChE può idrolizzare 600.000 molecole di ACh al minuto.
4.5 Ruolo di AChE
Figura 4.6
Un’importante famiglia di sostanze, una delle quali è la neostigmina, inibisce l’azione di AChE. La neostigmina blocca l’azione dell’AChE e quindi rende il potenziale della piastra terminale più grande e più lungo nella durata., Questa figura illustra due potenziali endplate. Uno è stato registrato in soluzione salina e curaro e un secondo registrato dopo l’aggiunta di neostigmina alla soluzione. (Il curaro viene aggiunto in modo che le proprietà dell’EPP possano essere studiate senza innescare un potenziale d’azione nella cellula muscolare.) Dopo l’applicazione della neostigmina il potenziale della piastra terminale è molto più grande e più lungo nella durata.
4.6 a Miastenia Grave
La miastenia grave è associata a grave debolezza muscolare a causa di una diminuzione del numero di recettori dell’acetilcolina nella cellula muscolare., Se il potenziale della piastra terminale è inferiore, il potenziale della piastra terminale non raggiungerà la soglia. Se non riesce a raggiungere la soglia, non ci sarà alcun potenziale d’azione nella cellula muscolare e nessuna contrazione del muscolo, che causa debolezza muscolare. Neostigmina e altri inibitori di AChE sono usati per trattare pazienti con miastenia grave. Questi agenti rendono la quantità di acetilcolina che viene rilasciata più efficacemente raggiungere i restanti recettori dell’acetilcolina.
4.,6b Agenti nervosi
Sebbene gli inibitori del DOLORE abbiano un importante valore terapeutico, alcuni inibitori sono stati e sono ancora usati come veleni. Alcuni inibitori del dolore come Soman e Sarin formano un blocco abbastanza irreversibile di dolore. Questo blocco porta a livelli estremi di ACh nella fessura sinaptica. Gli individui così avvelenati muoiono per convulsioni e spasticità muscolare, compresi i muscoli respiratori.
Figura 4.7
4.,7 Ionoforesi di ACh
La ionoforesi è una tecnica interessante che può essere utilizzata per testare ulteriormente l’ipotesi che ACh sia la sostanza neurotrasmettitore alla giunzione neuromuscolare. Se ACh è il trasmettitore che viene rilasciato da questa sinapsi, si potrebbe prevedere che dovrebbe essere possibile sostituire l’applicazione artificiale del trasmettitore per il normale rilascio del trasmettitore. Poiché ACh è una molecola caricata positivamente, può essere forzata da un microelettrodo per simulare il rilascio di ACh da un terminale presinaptico.
Figura 4.,8
In effetti, piccole quantità di ACh possono essere applicate in prossimità della giunzione neuromuscolare. La figura 4.8 confronta un EPP prodotto dalla stimolazione dell’assone motore e la risposta alle espulsioni di ACh. Il cambiamento potenziale sembra quasi identico al potenziale endplate prodotto dal normale rilascio di ACh. Questo esperimento fornisce supporto sperimentale per il concetto che ACh è il trasmettitore naturale a questa sinapsi.,
La risposta all’espulsione di ACh ha alcune altre proprietà interessanti che sono tutte coerenti con la natura colinergica della sinapsi nella giunzione neuromuscolare scheletrica. La neostigmina rende la risposta alla ionoforesi di ACh più lunga e più grande. Curare riduce la risposta perché compete con il normale legame di ACh. Se ACh viene espulso nella cellula muscolare, non succede nulla perché i recettori per l’acetilcolina non sono all’interno; sono all’esterno della cellula muscolare., L’applicazione dell’acetilcolina alle regioni del muscolo a partire dalla fine-piastra non produce risposta perché i ricevitori per l’ACh sono concentrati alla regione sinaptica.
Per testare la tua comprensione finora, considera come un agente come TTX influenzerebbe la generazione di un EPP e la risposta di una fibra muscolare all’applicazione ionoforetica di ACh? TTX non ha alcun effetto sulla risposta a ACh, ma blocca l’EPP. Il motivo per cui la risposta all’ACH non è influenzata è chiaro, ma molti si aspettano che se non vi è alcun effetto qui, non ci dovrebbe essere alcun effetto sul PPE., La tetrodotossina non influenza il legame dell’acetilcolina con i recettori e quindi non influenzerà la risposta all’applicazione diretta di ACh. Tuttavia, la tetrodotossina influenzerà la capacità di un potenziale d’azione da suscitare nell’assone motore. Se un potenziale d’azione non può essere generato nell’assone del motore, non può causare il rilascio del trasmettitore. Pertanto, la tetrodotossina abolirebbe totalmente il PPE. Il blocco non sarebbe dovuto ad un blocco di recettori ACh, ma piuttosto ad un blocco di qualche passo prima del rilascio del trasmettitore.
4.,8 Meccanismi ionici dell’EPP
Bernard Katz e i suoi colleghi sono stati pionieri nello studio dei meccanismi di trasmissione sinaptica alla giunzione neuromuscolare. Hanno suggerito che il canale aperto da ACh era uno che aveva uguale permeabilità sia a Na+ che a K+. Poiché era ugualmente permeabile a Na+ e K+, Katz suggerì che, come risultato dell’apertura di questi canali, il potenziale di membrana si sarebbe spostato verso 0 mV. (Un valore di alfa nell’equazione GHK uguale a uno, che quando sostituito nell’equazione, produce un potenziale di circa 0 mV.,)
Figura 4.9
L’esperimento mostrato nella figura a sinistra verifica quel concetto. La cellula muscolare è stata penetrata con un elettrodo di registrazione e un altro elettrodo che può essere collegato a una fonte di potenziale adatta per modificare artificialmente il potenziale di membrana. Normalmente, il potenziale di membrana è di circa -80 mV, viene aggiunta una piccola quantità di curaro in modo che l’EPP sia piccolo. Katz ha notato in questi esperimenti che la dimensione dell’EPP è cambiata radicalmente a seconda del potenziale della cellula muscolare., Se il potenziale di membrana viene spostato a 0 mV, non viene registrata alcuna variazione di potenziale. Se il potenziale di membrana è fatto + 30 mV, l’EPP è invertito. Quindi tre diversi stimoli producono potenziali endplate molto diversi l’uno dall’altro.
La mancanza di una risposta quando il potenziale è a 0 mV è particolarmente informativa. Considera perché non viene registrato alcun cambiamento potenziale. Presumibilmente, il trasmettitore viene rilasciato e si lega ai recettori., La semplice spiegazione per una mancanza di potenziale cambiamento è che il potenziale a cui l’apertura dei canali ACh stanno cercando di raggiungere è già stato raggiunto. Se il potenziale di membrana è reso più positivo di 0 mV, l’EPP viene invertito. Non importa quale sia il potenziale, il cambiamento di permeabilità tende a spostare il potenziale di membrana verso 0 mV! Se il potenziale di riposo è più negativo di 0 mV, c’è una deflessione verso l’alto. Se è più positivo, c’è una deflessione verso il basso. Se è già a 0 mV, non c’è deflessione.
Figura 4.,10
Questo potenziale è anche chiamato potenziale di inversione, perché è il potenziale in cui il segno del potenziale sinaptico si inverte. L’esperimento indica che, come risultato del legame ACh ai recettori, i canali specifici diventano ugualmente permeabili a Na+ e K+. Questo cambiamento di permeabilità tende a spostare il potenziale di membrana da dove si trova inizialmente verso un nuovo potenziale di 0 mV.
Perché il normale potenziale della piastra terminale non raggiunge mai effettivamente 0 mV?, Una ragione è che la sequenza di cambiamenti di permeabilità che sono alla base del potenziale d’azione “palude fuori” i cambiamenti prodotti dal PPE. Ma anche se un potenziale d’azione non fosse attivato, l’EPP non raggiungerebbe ancora 0 mV. Questo perché i canali ACh sono solo una piccola frazione del numero totale di canali nelle fibre muscolari. Sono presenti anche i canali K+ che conferiscono a una cellula muscolare il suo potenziale di riposo. Il loro compito è cercare di mantenere la cellula al potenziale di riposo.,
Il canale aperto da ACh è un membro di una classe generale di canali chiamati canali ligando-gated o recettori ionotropici. Come illustrato nella Figura 4.10, il sito di associazione del trasmettitore fa parte del canale stesso. Come risultato del legame del trasmettitore al recettore (generalmente sono necessarie due molecole), vi è un cambiamento conformazionale nella proteina che consente a una regione dei pori di aprirsi e agli ioni di fluire verso il basso i loro gradienti elettrochimici. Ulteriori dettagli del canale sono presentati nel Capitolo 11.,
Testare la Vostra Conoscenza
- Domanda 1
- Un
- B
- C
- D
Una placca motrice potenziale di cellule del muscolo scheletrico potrebbe in linea di principio essere prodotta da una diminuzione della permeabilità, in quale dei seguenti ioni(s)? (Supponiamo che ci sia una permeabilità iniziale finita a ciascuno degli ioni elencati di seguito e che siano presenti gradienti di concentrazione fisiologici.):
A. Na+
B. Na + e Ca2+
C. Ca2 +
D., K+
Un potenziale di piastra terminale in una cellula muscolare scheletrica potrebbe in linea di principio essere prodotto da una ridotta permeabilità a quale dei seguenti ioni? (Supponiamo che ci sia una permeabilità iniziale finita a ciascuno degli ioni elencati di seguito e che siano presenti gradienti di concentrazione fisiologici.):
A. Na+ Questa risposta NON è CORRETTA.
Un potenziale di piastra terminale è una depolarizzazione che viene normalmente prodotta dall’aumento simultaneo della permeabilità agli ioni sodio e potassio., Se ci fosse una diminuzione selettiva della permeabilità al sodio, tale diminuzione non porterebbe a una depolarizzazione. Piuttosto, porterebbe effettivamente a un’iperpolarizzazione perché l’alfa nell’equazione GHK sarebbe ridotta. Il rapporto tra la permeabilità al sodio e al potassio sarebbe favorito verso la permeabilità del potassio, spostando il potenziale di membrana verso il potenziale di equilibrio del potassio e producendo un’iperpolarizzazione.
B. Na+ e Ca2+
C. Ca2 +
D., K+
Un potenziale di piastra terminale in una cellula muscolare scheletrica potrebbe in linea di principio essere prodotto da una ridotta permeabilità a quale dei seguenti ioni? (Supponiamo che ci sia una permeabilità iniziale finita a ciascuno degli ioni elencati di seguito e che siano presenti gradienti di concentrazione fisiologici.):
A. Na+
B. Na+ e Ca2+ Questa risposta NON è CORRETTA.
Se la permeabilità al sodio e al calcio fosse diminuita, le loro conseguenze sarebbero simili a quelle nella scelta A. Diminuendo la permeabilità al sodio da sola tenderebbe a iperpolarizzare la cellula., Allo stesso modo, diminuendo la permeabilità al calcio potrebbe anche iperpolarizzare la cellula. Il potenziale di equilibrio del calcio è un valore molto positivo, e se ci fosse una certa permeabilità a riposo tonica al calcio, quella permeabilità contribuirebbe ad una depolarizzazione tonica del potenziale di membrana. Quindi, una diminuzione della permeabilità del calcio rimuoverebbe quell’effetto depolarizzante tonico e si tradurrebbe in un’iperpolarizzazione.
C. Ca2 +
D., K+
Un potenziale di piastra terminale in una cellula muscolare scheletrica potrebbe in linea di principio essere prodotto da una ridotta permeabilità a quale dei seguenti ioni? (Supponiamo che ci sia una permeabilità iniziale finita a ciascuno degli ioni elencati di seguito e che siano presenti gradienti di concentrazione fisiologici.):
A. Na+
B. Na+ e Ca2+
C. Ca2+ Questa risposta NON è CORRETTA.
Una diminuzione della permeabilità del calcio da sola produrrebbe, semmai, un’iperpolarizzazione. Vedi logica di risposta alla scelta B.
D., K+
Un potenziale di piastra terminale in una cellula muscolare scheletrica potrebbe in linea di principio essere prodotto da una ridotta permeabilità a quale dei seguenti ioni? (Supponiamo che ci sia una permeabilità iniziale finita a ciascuno degli ioni elencati di seguito e che siano presenti gradienti di concentrazione fisiologici.):
A. Na+
B. Na+ e Ca2+
C. Ca2+
D. K+ Questa risposta è CORRETTA!
Una diminuzione della permeabilità del potassio porterebbe ad una depolarizzazione simile a un potenziale di piastra terminale., Questo perché c’è a riposo una permeabilità tonica al potassio e al sodio. L’elevata permeabilità al potassio tende a mantenere il potenziale di membrana vicino al potenziale di equilibrio del potassio. Se quella permeabilità a riposo è diminuita, l’alfa nell’equazione di Goldman diventerebbe un valore maggiore, spostando il potenziale di membrana un po ‘ più vicino al potenziale di equilibrio del sodio (cioè una depolarizzazione).