Lewis structure of water molecule contiene due singoli legami attorno all’atomo di ossigeno. numero di elettroni di valenza totale di atomi di ossigeno e idrogeno sono utilizzati per disegnare la struttura di lewis. Ogni passo del disegno lewis struttura di H2O sono spiegati in questo tutorial.
H2O lewis structure
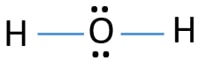
Nella struttura lewis di H2O, ci sono due singoli legami attorno all’atomo di ossigeno. Gli atomi di idrogeno sono uniti all’atomo di ossigeno attraverso singoli legami. Inoltre, ci sono due coppie solitarie sull’atomo di ossigeno.,
La molecola d’acqua è una molecola semplice. Disegno lewis struttura della molecola d’acqua è semplice rispetto ad alcune delle altre molecole complesse o ioni. Immagina di disegnare la struttura di lewis dello ion tiosolfato.
Passi per disegnare la struttura di lewis di H2O
Ci sono alcuni passi da seguire per disegnare correttamente una struttura di lewis. Per la molecola H2O, la sua struttura di lewis e questi passaggi sono spiegati in dettaglio in questo tutorial. Poiché la molecola d’acqua è semplice, alcuni di questi passaggi non vengono utilizzati molto. In tali casi, sono menzionati con i rispettivi passaggi.,
- Trova il numero totale di elettroni dei gusci di valance degli atomi di idrogeno e dell’atomo di ossigeno
- Coppie di elettroni totali come coppie e legami solitari
- Selezione dell’atomo centrale
- segna coppie solitarie sugli atomi
- Segna le cariche sugli atomi se ci sono.
- Controllare la stabilità e ridurre al minimo le cariche sugli atomi convertendo coppie solitarie in legami per ottenere la migliore struttura di lewis.
Importante: Disegnare correttamente la struttura di lewis è importante per disegnare correttamente le strutture di risonanza.,
Numero totale di elettroni dei gusci di valance di H2O
Ci sono due elementi; idrogeno e ossigeno. L’idrogeno è un elemento del gruppo IA e ha un solo elettrone nel suo ultimo guscio (guscio di valenza). L’ossigeno è un gruppo TRAMITE elemento nella tavola periodica e contiene sei elettroni nel suo ultimo guscio. Ora sappiamo quanti elettroni sono inclusi nei gusci di valenza di ciascun atomo.,
- elettroni di valenza dato dagli atomi di idrogeno = 1 * 2 = 2
- elettroni di valenza dato da atomi di ossigeno = 6*1 = 6
- Totale di elettroni di valenza = 2 + 6 = 8
Totale di elettroni di valenza di coppie
Totale valance coppie di elettroni = legami σ + π obbligazioni + lone pairs a valence conchiglie
Totale coppie di elettroni sono determinate dividendo il numero totale di elettroni di valenza per due. Per, H2O, le coppie totali di elettroni sono 4 nei loro gusci di valenza.,
Atomo centrale di H2O
Per essere l’atomo centrale, la capacità di avere una maggiore mantovana è importante. Quindi, dall’idrogeno e dall’ossigeno, quale atomo ha la valenza più alta? La valenza massima dell’ossigeno è due. l’unica valenza dell’idrogeno è una. Pertanto, l’atomo di ossigeno dovrebbe essere l’atomo centrale di H2O. Ora, possiamo disegnare uno schizzo di H2O per mostrare come gli atomi si trovano nella molecola.
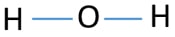
Coppie solitarie sugli atomi
Dopo aver determinato l’atomo centrale e lo schizzo della molecola H2O, dovremmo iniziare a segnare coppie solitarie sugli atomi., Ricorda che ci sono un totale di quattro coppie di elettroni.
- Ci sono già due legami H-O nella struttura dello schizzo disegnato. Ora rimangono solo due (4-2) coppie di elettroni da marcare sugli atomi.
- Di solito, quelle coppie di elettroni rimanenti dovrebbero essere iniziate a segnare su atomi esterni. Ma in H2O, atomo di idrogeno sono gli atomi esterni che non possono mantenere più di due elettroni nel suo ultimo guscio. Pertanto, non possiamo contrassegnare quelle coppie di elettroni sugli atomi di idrogeno.,
- Quindi, segna quelle due coppie di elettroni sull’atomo centrale; ossigeno

Segna le cariche sugli atomi
Non ci sono cariche sull’atomo di ossigeno e sugli atomi di idrogeno.
Controlla la stabilità e minimizza le cariche sugli atomi convertendo coppie solitarie in legami
Perché non ci sono cariche sugli atomi, non c’è bisogno di ridurre le cariche come passo per disegnare la migliore struttura di lewis. Già, abbiamo ottenuto la migliore struttura di lewis per H2O.
Domande
Quali sono le strutture di lewis simili all’acqua possono essere disegnate per?,
Nella struttura di lewis della molecola d’acqua, ci sono due legami sigma e due coppie solitarie intorno sulfuratom. L’idrogeno solforato, il difluoruro di ossigeno (F2O) hanno strutture di lewis simili all’acqua.
Fai le tue domande di chimica e trova le risposte
Tutorial correlati