HLA-B27 összefüggő akut anterior uveitis (KME) a leggyakoribb típus az endogén uveitis (lásd a lenti képet), a számviteli 18-32% – a az összes elülső uveitis esetekben a nyugati országokban, valamint a 6-13% – a az összes elülső uveitis esetekben Ázsiában. A viszonylag alacsonyabb gyakoriság Ázsiában a HLA-B27 alacsonyabb gyakoriságához kapcsolódik ebben a populációban., Mint már említettük, a HLA-B27 kapcsolódó AAU különböző globális mintái vannak, amelyek különböző genetikai tényezőknek tulajdoníthatók, például a HLA-B27 polimorfizmusoknak és a nem MHC géneknek. Ezek a földrajzi eltérések a még nem azonosított patogén környezeti tényezők miatt is létezhetnek.
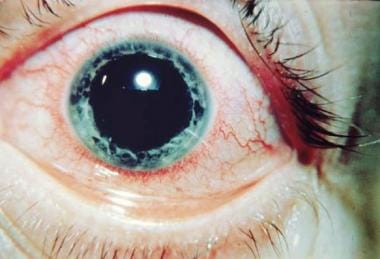 akut anterior uveitis spondylitis ankylopoeticában. Jóvoltából Paul Dieppe, BSc, MD, FRCP, FFPHM.,
akut anterior uveitis spondylitis ankylopoeticában. Jóvoltából Paul Dieppe, BSc, MD, FRCP, FFPHM., tanulmányok azt mutatják, hogy a HLA-B27 társult uveitis egy különálló entitás, amelyet a férfiak túlsúlya és gyakori társulása jellemez szeronegatív arthritises szindrómákkal, mint például spondylitis ankylopoetica, reaktív arthritis, arthritis psoriatica, és gyulladásos bélbetegség. A HLA-B27 társult AAU első epizódja leggyakrabban 20-40 éves betegeknél fordul elő, míg a HLA-B27-negatív AAU kialakulásának kora általában egy évtizeddel később fordul elő. Az AAU-ban szenvedő betegek 50-60% – a lehet HLA-B27 pozitív., Ez általában egy jóindulatú nongranulomatous egyoldalú betegség, amely a fájdalom, a vörösség és a fotofóbia klasszikus hármasaként jelenik meg.
a szaruhártya-megnyilvánulások közé tartozhat a finom keratitikus csapadék és az endotélium fibrinje. A szaruhártya ödémája endotheliális kompromisszum és dekompenzáció következménye lehet. Band keratopathia, a kalcium felhalmozódása a szaruhártya epitéliumában, krónikus uveitisben fordulhat elő., Az elülső kamra azt mutatja, sejtek, illetve napkitörés, amely egy haze láttam a réslámpa vizsgálat, ami a fehérje felhalmozódását az elülső kamra miatt a bontás, a vér-vizes akadály, illetve súlyos gyulladás, fibrinous váladékot az elülső kamra elzárhatja a tanuló, ami iris bomba, mint látható az alábbiakban. Ez a fibrin összetéveszthető endogén endophthalmitissel, szürkehályoggal vagy hypopyonnal. Hypopyon látható, ritkán spontán hyphema is előfordul a súlyosan dilatált írisz hajók következtében.,
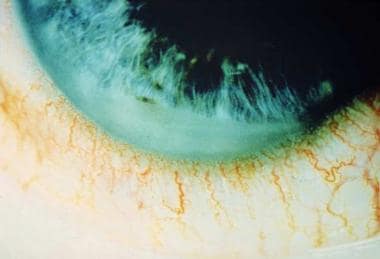 anterior chamber fibrin collection in ankylosing spondylitis. Jóvoltából Paul Dieppe, BSc, MD, FRCP, FFPHM.
anterior chamber fibrin collection in ankylosing spondylitis. Jóvoltából Paul Dieppe, BSc, MD, FRCP, FFPHM. Pigment diszperzió, pupilláris miózis és iris csomók figyelhetők meg, valamint szinechiák fordulhatnak elő mind az elülső, mind a hátsó részen. A hátsó szegmens bevonása viszonylag ritka, de cisztoid makula ödéma, lemezödéma, pars plana exudátumok vagy choroiditis látható. A szemnyomás gyakran alacsony, másodlagos csökkent vizes termelés-gyulladás a sugártest, valamint trabecularis kötőelemek., Szemnyomás is magas lehet, ha gyulladásos sejtek, illetve törmelék eltömítheti a trabecularis kötőelemek, különösen a betegek már létező szegény létesítmény a kiáramlás.
AAU általában rövid, néhány naptól hetekig, legfeljebb 3 hónapig tart, hajlamos ugyanabban a szemben megismétlődni, különösen azoknál az egyéneknél, akik HLA-B27 pozitívak. Az AAU szövődményei közé tartozik a szürkehályog, a glaukóma, a hipotónia, a cisztoid makula ödéma és a szinechiák kialakulása., A HLA-B27-hez társuló elülső uveitis prognózisa szisztémás betegséggel vagy anélkül kevésbé kedvező, összehasonlítva azokkal a betegekkel, akik idiopátiás anterior uveitis esetén HLA-B27 negatívak. A következmények lehetősége ellenére az általános prognózis jó.
A Classic AAU teljesen megszűnik, ha azonnal és agresszíven kezelik. Az alulkezelt vagy rosszul diagnosztizált esetek a vér-vizes gát tartós károsodása miatt krónikus iridociklitishez vezethetnek.,
diagnózis
a gondos anamnézis és a fizikális vizsgálat általában segít megkülönböztetni a szisztémás betegséggel összefüggő uveitikus entitásokat és a HLA-B27-et azoktól, amelyek nem kapcsolódnak a HLA-B27-hez. Az AAU-t okozó betegségek változatosak, beleértve a traumás iritis, postcataract extraction iritis, juvenilis rheumatoid arthritis, herpeszes fertőzés (mind a herpes simplex, mind a herpes zoster), szifilisz, szarkoidózis, Fuchs heterokróm iridociklitis, glaukomatociklitikus válság, Behcet-betegség és alacsony minőségű endophthalmitis.,
az egyoldalú AAU-ban szenvedő betegeknél a HLA-B27 vizsgálat szerepe fontos a differenciáldiagnózisban. A HLA-B27 antigén hiánya az egyoldalú AAU-ban nyom lehet a klinikus számára, hogy más specifikus uveitis entitásokat és más szisztémás betegségeket keressen. Hasznos lehet az AAU prognózisának meghatározásában is, mivel a HLA-B27-hez kapcsolódó AAU, még szisztémás betegség hiányában is, kevésbé kedvező és valószínűbb, hogy megismétlődik, összehasonlítva a HLA-B27 negatív betegekkel.,
kezelés
az AAU orvosi kezelése helyi vagy szisztémás kortikoszteroidokat és helyi cikloplegikákat tartalmaz. A periokuláris kortikoszteroid injekciók rendkívül hasznosak akut, ellenszenves vagy nem megfelelő esetekben, különösen akkor, ha a hátsó szegmens bevonása történik. Immunszuppresszív kezelésre lehet szükség refrakter esetekben vagy kortikoszteroid által kiváltott káros hatásokkal rendelkező betegeknél. Az elsődleges cél az összes sejt kiküszöbölése, ezáltal minimalizálva a szövődményeket, beleértve a szürkehályogot, a cisztoid makula ödémát, a hipotóniát, a szinechiák kialakulását vagy a glaukómát.,
a Cikloplegikumok enyhítik a ciliáris görcs okozta fotofóbiát, megakadályozzák és megszakítják a szinechiák kialakulását. A legtöbb esetben elegendő a rövid hatású cseppek, például 1% ciklopentolát-hidroklorid vagy 1% tropikamid. Ezek lehetővé teszik a pupilláris motilitást és a gyors gyógyulást, ha abbahagyják. Hosszabb hatású cikloplegikumok, például 5% homatropin, 0,25% szkopolamin és 1% atropin szintén hasznosak lehetnek. Ha az uveitis súlyosabb, a cikloplegikumok gyakoribb adagolására lehet szükség.,
a lokális kortikoszteroidok képezik az uveitis terápia alapját, de káros hatásaik miatt körültekintően kell alkalmazni őket. A cél a gyulladás szabályozásához és a szövődmények megelőzéséhez szükséges minimális mennyiség alkalmazása. Az agresszív kezdeti terápia felgyorsíthatja a gyógyulást és korlátozhatja a kezelés időtartamát. A prednizolon-acetát óránként adott 1% Erősen ajánlott akut prezentációkhoz. Általában 2-3 hét maximális gyakorisággal minden, ami szükséges az összes sejt teljes eltávolításához. A kortikoszteroidokat mindig hagyja abba az adag csökkentésével.,
a kortikoszteroidok 4 módon adhatók, beleértve a lokális, periokuláris, intraokuláris (intravitrealis) és szisztémás kezelést. A helyi terápiát az elülső uveitisben alkalmazzák. Az adagolás óránként változik naponta egyszer. A kenőcs formája azok számára áll rendelkezésre, akik nem tolerálják a tartósítószert a cseppekben, és különösen hasznosak lehetnek a hosszabb hatású esti adagoláshoz. Előfordulhat, hogy a súlyos gyulladás nem reagál, és periokuláris, intraokuláris vagy szisztémás kortikoszteroidokat igényelhet, különösen, ha a hátsó szegmens érintett., A periokuláris kortikoszteroidokat általában depot injekcióként adják be az Al-Tenon térben.
intravitrealis kortikoszteroidok injekcióval vagy tartós felszabaduló eszköz beültetésével hasznosnak bizonyultak mind a krónikus uveitis, mind az uveitic cystoid macularis ödéma kezelésében. Ezek a tartós eszközök különösen ígéretesek a hosszú távú gyulladás kezelésében, mivel a beültetés után akár több évig is felszabadíthatják a gyógyszereket., Ez lehetővé tenné a szisztémás kortikoszteroidok vagy immunszuppresszív szerek csökkentését vagy eltávolítását, ezáltal minimalizálva az ezekkel a szerekkel történő kezeléssel kapcsolatos káros hatásokat. Mint minden kortikoszteroid kezelés esetében, az intraokuláris nyomást rendszeresen ellenőrizni kell.
a szisztémás kortikoszteroidok orálisan vagy intravénásan adhatók be. Ezek különösen akkor előnyösek, ha a szisztémás betegség terápiát is igényel. Fontos, hogy megbeszéljük a kortikoszteroidok káros hatásait a beteggel, és hogy ezeket a beteg alapellátási orvosa ellenőrizze., Az 1 mg/kg/d prednizon hasznos kezdő adag.
Több erős immunszuppresszió szükség lehet a betegek látást veszélyeztető gyulladás zavarja a mindennapi tevékenységeket, válasz hiánya kortikoszteroid kezelés, valamint az intolerancia, a kortikoszteroidok. Azok a betegek, akik 10 mg-ot vagy annál többet szednek a tüneteik kezelésére, biztonságosabb hosszú távú kezelésként részesülhetnek antimetabolitból. Az ilyen helyzetekben alkalmazott gyógyszerek közé tartoznak azatioprin, mikofenolát-mofetil, ciklofoszfamid, klórambucil, metotrexát, takrolimusz és ciklosporin., Ezeket a szereket általában a posterior uveitisben vagy panuveitisben alkalmazzák, de alkalmanként szükség lehet a reaktív ízületi gyulladással vagy spondylitis ankylopoeticával járó súlyos fibrinos anterior uveitisre.
a ciklosporin egyre hasznosabbá válik a szisztémás kortikoszteroidok kiegészítéseként. Lehetővé teheti az orvos számára, hogy a remisszió elérése után csökkentse vagy teljesen visszavonja a kortikoszteroidokat. A szokásos adag 2,5-5 mg/kg/d. A vérnyomás és a vesefunkció gondos monitorozása szükséges., A vizsgálati terápiák közé tartozik a ciklosporint vagy a fluocinolont erősen lipidoldható szteroidot tartalmazó tartós felszabadulású eszköz és a CD4 molekula elleni monoklonális antitestek.
az uveitis jelenlegi terápiái hatásmechanizmusukban nem specifikusak, és számos káros hatásuk van, amint azt már említettük. Ennek köszönhetően számos immunmodulációval foglalkozó terápiát vizsgáltak. Két ígéretes kezelés a tumorellenes nekrózis faktor alfa (anti-TNF-alfa) és a HLA-B27 orális tolerancia terápia alkalmazása., A TNF-alfa mind állatkísérletekben, mind humán kísérleti vizsgálatokban kimutatták, hogy az uveitis különböző formáinak, köztük az AAU-nak a patogenezisében kritikus gyulladásos felbujtó. Ennek fényében vizsgálatokat végeztek az anti-TNF-alfa alkalmazásának hatékonyságára és biztonságosságára az uveitis különböző formáinak kedvező eredményekkel történő kezelésében. Az Infliximab egy Murin-humán kiméra monoklonális antitest, amely a humán TNF-alfa ellen irányul., Kimutatták, hogy a Behcet-kórban és a refrakter posterior uveitisben a látást veszélyeztető szemgyulladás gyors, hatékony és biztonságos kezelése.a
az Etanercept géntechnológiával módosított fúziós fehérje, amely mind a TNF-alfát, mind a TNF-béta-t megköti és inaktiválja., Egy tanulmány kimutatta, hogy a hatékonyság a fehérje javítja mindkét szemészeti gyulladás, ízületi gyulladás, amikor szubkután kétszer egy héten legalább 3 hónappal a kezelés ellenálló krónikus uveitis, beleértve a krónikus anterior uveitis a gyermekek juvenilis rheumatoid uveitis, valamint idiopathiás uveitis. Ez lehetővé tette mind a szisztémás kortikoszteroidok, mind a szisztémás metotrexát csökkentését.
az orális tolerancia magában foglalja egy antigén szájon át történő beadását, hogy specifikus perifériás immuntoleranciát indukáljon., Az orális tolerancia mechanizmusai nem egyértelműek, de úgy gondolják, hogy egy specifikus antigént, valamint az antigén dózisától függő aktív szuppresszió vagy klonális anergia generálását foglalja magában. Orális tolerancia kimutatták, hogy sikeres kísérleti modellek foglalkozó sclerosis multiplex, ízületi gyulladás, cukorbetegség, myasthenia gravis, uveitis., Ennek alapján klinikai vizsgálatokat indítottak olyan antigének alkalmazásával, mint a myelin a sclerosis multiplexben, a rheumatoid arthritisben lévő kollagén és az uveitogén peptidek az intermedier és posterior uveitisben, ismét sikerrel és a kezelés néhány káros hatásával. A retina autoantigént utánzó HLA-B27-ből származó peptid (b27pd) hatásosnak bizonyult mind az állati modellekben, mind az uveitisben szenvedő betegekben.
egyéb feltörekvő terápiás lehetőségek közé tartozik az antibiotikum terápia, tekintettel a gram-negatív bakteriális fertőzések HLA-B27 társult AAU kiváltásakor játszott szerepére., A szulfaszalazin-kezelést megvizsgálták annak lehetséges szerepe miatt az AAU visszatérő támadásainak számának csökkentésében, és profilaktikus ciprofloxacint is vizsgáltak, de nem találták előnyösnek a káros hatások és költségek miatt.
a jövőbeni új lehetséges kezelések az immunrendszer jobb megértésén alapulnak, és olyan anyagokat fognak tartalmazni, mint a citokinek, a kemokinek, a sejt tapadásmolekulák és a T-sejtek alcsoportjai.,
a reumatológus szerepe az AAU kezelésében fontos szerepet játszik a jelen lévő szisztémás betegségek azonosításában és a későbbi immunszuppresszív terápia monitorozásában.