Lewis structure of water molecule sisältää kaksi yksittäistä sidosta happiatomin ympärillä. hapen ja vetyatomien kokonaisvalenssielektronien lukumäärää käytetään Lewisin rakenteen piirtämiseen. Jokainen vaihe piirustus lewis rakenne H2O selitetään tässä opetusohjelma.
H2O lewis rakenne
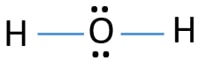
Vuonna lewis rakenne, H2O, on olemassa kaksi erillistä joukkovelkakirjoja noin happiatomi. Vetyatomit yhdistyvät happiatomiksi yksittäisten sidosten kautta. Happiatomilla on myös kaksi yksinäistä paria.,
vesimolekyyli on yksinkertainen molekyyli. Vesimolekyylin Lewis-rakenteen piirtäminen on yksinkertaista kuin joidenkin muiden monimutkaisten molekyylien tai ionien. Kuvitelkaa tiosulfaatti-ionin Lewis-rakenne.
Lewisin rakenteen piirtämisen vaiheet H2o
on joitakin vaiheita, joiden jälkeen lewis-rakenne piirretään kunnolla. H2o-molekyylille sen lewis-rakenne ja nämä vaiheet selitetään yksityiskohtaisesti tässä opetussuunnitelmassa. Koska vesimolekyyli on yksinkertainen, osaa näistä vaiheista ei juuri käytetä. Tällaisissa tapauksissa, ne on mainittu kunkin vaiheet.,
- Etsi yhteensä määrä elektroneja valance kuoret vetyatomia ja happiatomi
- Yhteensä elektronit paria niin yksinäinen paria ja joukkovelkakirjoja
- Center atom-valinta
- merkki yksinäinen paria atomien
- Merkki maksuja atomien jos on.
- Tarkista atomien Stabiilisuus ja minimoi lataukset muuntamalla yksinäiset parit sidoksiksi parhaan lewis-rakenteen saamiseksi.
Tärkeää: Piirustus oikea lewis rakenne on tärkeää kiinnittää resonanssi rakenteita oikein.,
Yhteensä määrä elektroneja valance kuoret H2O
On olemassa kaksi elementtiä; vety ja happi. Vety on ryhmän IA alkuaine ja sen viimeisessä kuoressa (valence shell) on vain yksi elektroni. Happi on ryhmä alkuaineen kautta jaksollisessa järjestelmässä ja sisältää sen viimeisessä kuoressa kuusi elektronia. Nyt tiedämme, kuinka monta elektronia on mukana jokaisen atomin valenssikuorissa.,
- valence elektronit antama vetyatomit = 1 * 2 = 2
- valence elektronit antama happiatomia = 6*1 = 6
- Yhteensä valence elektroneja = 2 + 6 = 8
Yhteensä valence elektronit paria
Yhteensä valance elektronit paria = σ joukkolainat + π joukkolainat + lone pairs at valence kuoret
Yhteensä elektroni paria määritetään jakamalla määrä yhteensä valence elektronit kaksi. Sillä, H2O, yhteensä elektroniparit ovat 4 niiden valenssi kuoret.,
Center atom H2O
olla keskellä atom, kyky ottaa suurempi helma on tärkeää. Sitten vedystä ja hapesta, millä atomilla on korkein valenssi? Hapen maksimivalenssi on kaksi. vedyn ainoa valenssi on yksi. Sen vuoksi happiatomin pitäisi olla H2O: n keskusatomi, Ja nyt voimme piirtää H2O: sta piirroksen, joka osoittaa, miten atomit sijaitsevat molekyylissä.
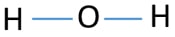
Yksinäinen paria atomien
Kun määritetään center atom ja luonnos H2O-molekyyli, meidän pitäisi alkaa merkitä yksinäinen paria atomeja., Muista, että elektronipareja on yhteensä neljä.
- piirretyssä sketsirakenteessa on jo kaksi H-O-sidosta. Nyt atomeihin on jäljellä enää kaksi (4-2) elektroniparia.
- yleensä nuo jäljellä olevat elektroniparit pitäisi alkaa merkitä ulkopuolisiin atomeihin. Mutta H2o: ssa vetyatomi on ulkoatomeja, jotka eivät voi pitää enempää kuin kahta elektronia viimeisessä kuoressaan. Siksi emme voi merkitä näitä kahta elektroniparia vetyatomeille.,
- Sitten, merkitse ne kaksi elektronia paria center atom; hapen

Mark maksuja atomien
ei ole mitään maksuja happiatomin ja vetyatomien.
Tarkista vakautta ja vähentää maksuja atomien muuntamalla yksinäinen paria joukkovelkakirjoja
Koska ei ole maksuja atomeja, ei tarvitse vähentää maksuja askel piirustus paras lewis-rakenne. Jo, meillä on paras lewis rakenne H2O.
Kysymyksiä
Mitä ovat samanlaisia lewis rakenteita vettä voidaan tehdä?,
vesimolekyylin Lewis-rakenteessa on kaksi sigma-sidosta ja kaksi yksinäistä paria sulfuratomin ympärillä. Vetysulfidilla, happidifluoridilla (F2O) on samanlaiset lewis-rakenteet kuin vedellä.
Kysy kemian kysymyksiä ja löydä vastaukset
Aiheeseen liittyvät oppaat