biologiske terapier omfatter en bred vifte af medicinske produkter. Vacciner, blodprodukter og stamcelleinjektioner er eksempler på første generations biologiske terapier. Men når folk taler om “biologics”, betyder de normalt andengenerations biologiske terapimedikamenter som Humira, Remicade og Enbrel.
se Biologics for RA og andre Autoimmune tilstande
biologiske responsmodifikatorer kan anvendes til behandling af inflammatoriske autoimmune sygdomme, såsom reumatoid arthritis og ankyloserende spondylitis., Læs Biologics: grundlæggende fakta for patienter
biologiske terapier (både første og anden generation) kan ikke fremstilles ved hjælp af en simpel kemisk reaktion, såsom blanding af ingredienser sammen i et laboratorium, den måde konventionelle lægemidler fremstilles på. I stedet fremstilles biologiske terapier ved hjælp af levende organismer, såsom bakterier, gær og endda pattedyrvæv og celler.
Making Biologics
biologiske lægemidler fremstilles ved hjælp af meget komplekse fremstillingsprocesser, der involverer levende celler.,
mens fremstillingsmetoder kan variere, fremstilles de fleste biologiske produkter, der sælges i dag til behandling af inflammatorisk ledsmerter, ved hjælp af disse grundlæggende trin:
- et stykke DNA indsættes i en levende celle—en gær -, bakterie -, viral-eller pattedyrscelle.
- DNA-stykket instruerer cellen til at producere en stor mængde af et specifikt molekyle, normalt et protein.
- molekylerne isoleres derefter, så alle levende celler og andet materiale er væk, og kun de ønskede molekyler er tilbage.
- de isolerede molekyler bliver den aktive ingrediens i et biologisk lægemiddel.,
molekyler i en biologisk lægemiddel er forskellige fra molekyler i de fleste andre farmaceutiske produkter på grund af deres store størrelse, mangel på ensartethed, og svage kemiske bindinger:
i Stor størrelse og manglende ensartethed
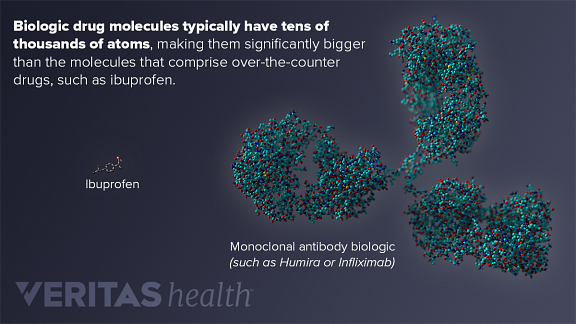
De molekyler, der udgør en biologisk lægemiddel ikke er lige det samme, og hvert molekyle, der typisk har titusinder atomer.
svage kemiske bindinger
de kemiske bindinger, der holder disse molekyler sammen, er relativt svage. Molekylerne kan nedbrydes, hvis de udsættes for hurtige temperaturændringer og andre faktorer.,
da molekylerne, der udgør biologiske stoffer, er så følsomme, skal producenterne følge specifikke trin for at fremstille og pakke et biologisk produkt. Selv små forskelle i fremstillings—og emballeringsprocessen—såvel som opbevaring og administration-af en biologisk kan påvirke et lægemiddels evne til at arbejde.
 Gem
Gem FDA-Godkendelse af bioteknologiske produkter
Når FDA godkender en konventionel medicin, er det vurderer stoffets kemiske egenskaber, styrke og impuritiessuch som, hvor mange kulstofatomer, det indeholder., Denne type evaluering kan ikke gøres med biologics: deres molekylers variation og store størrelser gør det umuligt for forskere at analysere og præcist beskrive hvert molekyle i et biologisk lægemiddel.
se risici og bivirkninger ved Biologics
da biologiske stoffer er vanskelige at karakterisere, er FDA-godkendelsen af et biologisk lægemiddel baseret på dets fremstillingsproces. FDA gennemgår processen for at sikre, at slutproduktet er konsistent, og der er ingen væsentlige variationer mellem en batch og en anden., Center for Biologics Evaluation and Research (CBER) er ansvarlig for at sikre sikkerheden og effektiviteten af de biologiske produkter.